强大的蛋白质促进损伤后周围神经的再生和生长
外周神经系统是一种庞大的神经网络,主要存在于大脑和脊髓外,并连接到身体的远达。周围的外周神经使它们变得非常容易受到血液伤害,切割和腿部和腿部骨折的伤害,以及疾病,以及疾病,患有糖尿病,Charcot-Marie-tooth和Guillain-Barre综合征。与中枢神经系统(脑和脊髓)不同,周围神经确实具有再生的能力,炎症免疫应答在再生中发挥着关键作用。
案例西部储备大学医学院科学家已经在实验室动物中展示了特定信号蛋白的再生动态,C-C类化学因子2(CCL2)。CCL2将炎症免疫细胞(巨噬细胞)发送给外周神经细胞簇,以促进修复并触发基因表达,导致神经细胞的新生长。研究结果在11月中旬在线发布,并将出现在2016年1月发布的问题实验神经病学。
“我们对我们的发现感到兴奋,因为我们没有理由期望仅仅表达趋化因子CCL2就足以刺激神经再生Richard E. Zigmond博士,凯斯西储大学医学院神经科学和病理学教授。“CCL2如此强大,这是很了不起的。”
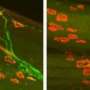
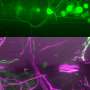
损伤后,CCL2影响外周神经细胞簇的工作,称为神经节,神经纤维远离损伤部位。每个外周神经电池具有主体和尾部状延伸,称为轴突。为了感觉神经细胞,轴突在离开细胞体后分裂,其中一部分从神经细胞体投射出来捕捉感觉,而另一部分将信息传送到脊髓和大脑。
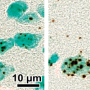
经过一个地区受伤周围神经, CCL2向巨噬细胞发出信号,使其移动到受损的轴突区域,清除细胞碎片,为新轴突的生长扫清道路。CCL2还向巨噬细胞发出信号,使其进入损伤的神经节区域,该区域容纳单个神经细胞,促进神经再生。至少在一定程度上,再生也会发生,因为巨噬细胞会触发促进新轴突生长的基因。
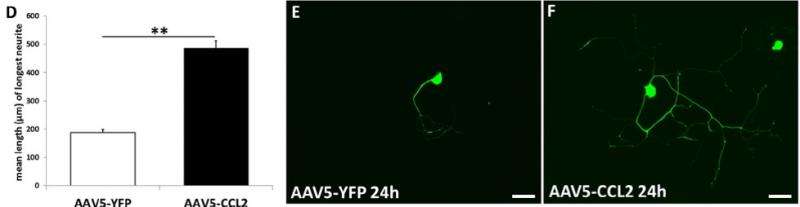
Zigmond最近的研究表明了这种CCL2机制在实验室动物的工作。在一个实验中,高级研究生Jon Niemi注入野生型,未加注的小鼠旨在触发CCL2表达的病毒。这些小鼠中CCL2表达的增强导致巨噬细胞的大累积三周后,在背根神经节,一簇感觉神经细胞它既可以延伸到外周区域,也可以延伸到中枢神经系统。更多的巨噬细胞积聚,反过来,产生更大的神经元发芽,神经再生的开始。
然而,这种经验完全不同于缺乏能够通过CCL2的受体(CCR2)的小鼠。没有受体,在CCR2缺陷小鼠中,巨噬细胞积累中的相同尖峰根本不会发生。这些动物仅具有瘢痕神经生长,其几乎与在野生型小鼠中观察到的神经再生并没有。
“我们在另一种类型的老鼠中做了同样的实验,发现了相同的相关性,”Zigmond说。“如果巨噬细胞没有进入神经节,则大大阻碍了再生。我们发现了感觉和交感神经神经元的真实。我们得出结论,巨噬细胞进入神经节和神经再生之间存在相关性。”
研究人员还证实了CCL2过表达在基因表达改变中的作用。
通过在动物中筛选与神经再生相关的mRNA分子来测试某些基因表达的调查,其中CCL2过表达促使神经元过剩。一种mRNA和一种蛋白质出现的白血病抑制因子(LIF)mRNA和神经元PSTAT3的变化(信号传感器和转录3)。这些特殊分子通过表达对指示神经元生长重要的基因来作用。通过引起巨噬细胞累积,CCL2增加了LIF mRNA和PSTAT3的水平,这导致背根神经节神经元的再生能力增加。为了测试其假设,该组使用STAT3激活的抑制剂阻止了LIF信号传导的激活。尽管CCL2通常增加,但抑制Stat3活化不会导致神经突生长的增加,这通常会增加背根神经节神经元的生长。
齐蒙德和其他研究人员的发现为炎症问题提供了新的思路。而不是一开始就对抗炎症周围神经损伤,可能允许有限的炎症损伤后可能是治疗刺激神经元再生。这些关于CCL2的发现也暗示了影响周围神经的疾病。
“我们的结论是免疫系统和神经系统以有益的方式互动,以产生巨噬细胞诱导的炎症和促进神经再生,”Zigmond说。“这在细胞体周围发生。响应于巨噬细胞活性的细胞内发生一些事情,除了巨噬细胞动作对损坏的远端神经轴突”。
加入Zigmond和该研究的主要作者Niemi是来自凯斯西储大学医学院神经科学系的贡献作者Alicia DeFrancesco-Lisowitz, Jared Cregg和Madeline Howarth。
进一步探索











用户评论