科学家揭示了β-淀粉样蛋白可能导致阿尔茨海默氏症
斯坦福大学医学院的科学家们已经表现出一种称为β-淀粉样蛋白的蛋白质片段,强烈涉及阿尔茨海默病,开始破坏突触,然后将其丛丛入斑块导致神经细胞死亡。
阿尔茨海默氏症影响了大约500万美国人,它的主要特征是大规模的损失突触- 联系地点神经细胞中继信号彼此 - 并平行劣化脑功能,特别是能够记住的能力。
“我们的发现表明阿尔茨海默病开始于之前的表现斑块形成神经生物学和生物学教授,一项研究的高级作者卡拉·沙茨博士说,该研究将于9月20日发表于《科学》杂志科学。
哈佛大学的调查人员也为这项研究做出了贡献。在小鼠和人类脑组织中进行的研究可能有助于解释近年来大规模临床试验的故障,试图通过药理学释放淀粉样蛋白斑块的脑来减缓阿尔茨海默氏症的进展。它还可能指出了在疾病早期阶段更好地治疗的方式。
β-淀粉样蛋白开始作为孤立分子的寿命,但倾向于最初堆积到仍然可溶的小簇中并且可以在大脑中自由行进,最后进入阿尔茨海默氏症的标志的斑块。该研究表明,在这种聚类形式中,β-淀粉样蛋白可以强烈地与神经细胞上的受体粘合,在运动中设置细胞间过程,其与其他神经细胞侵蚀其突触。
突触是神经细胞之间的连接。它们对于储存回忆,加工思想和情绪,以及计划和排序我们的身体是必不可少的。此外,这些连接的相对强度可以响应而改变新经验。
使用实验性小鼠菌株对阿尔茨海默病的突触和认知损伤感到高敏,Shatz和她的同事们表明,如果这些小鼠缺少平时靠近突触的表面蛋白,它们对内存分解和突触损失有关随着疾病。该研究首次证明该蛋白质称为PIRB,是β-淀粉样蛋白的高亲和力受体,其“可溶性簇”形式是β-淀粉样蛋白,其意味着可溶性β-淀粉样蛋白簇粘附到PIRB。这促进了一项级联的生物化学活动,最终突破突触突触。
Shatz是Sapp家族派大教授,以及Bio-X总监,一个关于医疗,工程和生物教师的大型斯坦福跨学科联盟绘图。她一直在研究PIRB多年,但在不同的背景下。在早期的工作中,Shatz使用缺乏它的转基因小鼠探讨了PiRB在大脑中的作用。她发现PIRB,以前认为只有免疫系统中的细胞仅用于大脑中的神经细胞,在那里它减慢了突触与它们所订婚的程度成比例的突触的能力,实际上促进他们的弱化。这种制动器在大脑中是理想的,因为太容易的突触强度 - 移位可能会引发像癫痫一样的不足的后果。
在新的研究中,Shatz的团队使用了一种不同的基因工程小鼠,它的基因组包含两个独立的人类基因的突变副本。这些突变中的每一种都被认为容易使人患上阿尔茨海默病。当这两种突变都出现在小鼠身上时,通常不会发生淀粉样蛋白斑块,结果是具有前进年龄的丰富淀粉样蛋白斑块沉积,以及在各种记忆测试中的性能下降的最终下降。
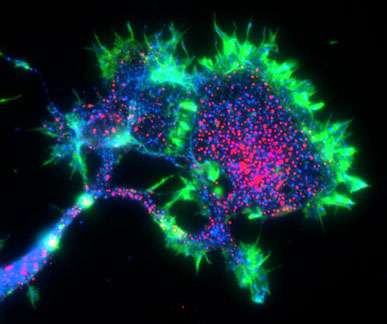
“我一直发现这些小鼠的奇怪 - 事实上,除了阿尔茨海默氏病的所有小鼠模型,我们和其他人的研究 - 似乎没有任何困难的问题,直到他们变老,”Shatz说。“这些小鼠的大脑在很小时期具有高水平的β-淀粉样蛋白。”
沙茨发现自己在想,是否可能有一种更敏感的方法来测量-淀粉样蛋白对年轻大脑的早期影响。2012年,她与人合作完成的一项研究表明,老鼠大脑的一个特定区域,其组成突触在应对早期生活经历时通常相当灵活,但在年轻易患阿尔茨海默氏症的老鼠身上却没有这种灵活性。这表明,与阿尔茨海默氏症相关的微妙影响可能比斑块或记忆丧失出现得更早。
现在,Shatz想知道从阿尔茨海默鼠标应变中消除PIRB是否可以恢复这种灵活性。因此,她的团队将Alzheimer的基因携带菌株与PIRB缺失的菌株培养,以产生杂种。实验表明,年轻的“阿尔茨海默氏鼠”的大脑,其中不存在PIRB的突触强度转化为正常小鼠的突触强度。由于正常的小鼠在成熟的记忆测试中,缺乏阿尔茨海默氏老鼠也表现成了成年人,而他们否则相同的PIRB表达的同伴遭受了大量突触和记忆损失。
“缺乏皮尔b的阿尔茨海默氏症小鼠免受基因突变产生β -淀粉样蛋白的影响,”Shatz说。现在的问题是,为什么?
泰勒金,博士,Shatz实验室的博士后学者和新研究的主要作者,他在2011年烹制了他对一名其有的一个 - 4岁儿子的俘虏观众的研究他开车去蒙特雷湾水族馆:也许pirb和β-淀粉样蛋白是结合的。这可能会导致PIRB在刹车上踩踏而不是通常这样做,因此它们可以完全消失,削弱突触,并与他们一起回忆。
进一步的实验表明,实际上,β-淀粉样蛋白强烈地结合到PIRB中。虽然PiRB特别是小鼠蛋白质,但KIM也首次鉴定为人脑中的类似β-淀粉样蛋白受体:一种叫做LILRB2的蛋白质。
在另一个实验中,Kim比较了缺乏pirb的老年痴呆症小鼠和表达pirb的老年痴呆症小鼠大脑中的蛋白质。后者显示出一些重要蛋白质的活性显著增加,特别是一种叫做cofilin的酶。随后的研究还发现,被解剖的阿尔茨海默氏症患者大脑中的cofilin活性远高于正常人。
在这里,曲线增厚:辛苷通过分解肌动蛋白,是对维持突触结构必然的建筑物嵌段蛋白。并且,随着新的研究表明,β-淀粉样蛋白与PIRB的结合导致生物化学变化对辛林,其转化其肌动蛋白破坏,突触拆卸活动。
“没有肌动蛋白,没有突触,”Shatz说。
金的假设似乎是正确的。β-淀粉样蛋白与PIRB结合(以及,研究人员证明,以其人类类似物,LILRB2),促进植物蛋白活动和破坏突触的结构完整性。
尽管可能有其他的破坏途径迫使突触行走,Shatz怀疑有很多。她说,她认为β -淀粉样蛋白和cofilin的直接参与,如此明显地与突触破裂有关,这表明这一途径是重要的。她说:“在这项研究中,我们也观察了人类的大脑,我们发现阿尔茨海默氏症患者的大脑中也存在类似的cofilin活性紊乱,但健康的大脑不是这样。”
Shatz认为,阻断-淀粉样蛋白在神经细胞表面与PirB结合的药物——例如,含有部分分子的可溶性PirB片段可以作为诱饵——可能会产生治疗效果。她说:“我希望这一发现对制药和生物技术公司具有足够的吸引力,有人会尝试推动这一想法。”











用户评论