FDA旨在改变它监视的方式去纤颤器的安全
去纤颤器应该拯救生命的令人震惊的病人的心脏恢复窦性心律,但自2005年以来,对45000例发生故障,根据美国食品和药物管理局。周五,美国食品和药物管理局提出新规则旨在确保潜在的救生设备正常工作时需要的。
FDA的计划是要求制造商自动体外除颤器或aed,提交申请上市前批准,根据这个公告。允许该机构“更密切关注这些设备是如何设计和制造的,”据FDA公告。
aed便携设备用于治疗的受害者心脏骤停一个条件,“心脏突然和意外停止跳动,”剥夺大脑和其他重要器官的血,根据国家心脏,肺和血液研究所。病人死如果他们不治疗通常在几分钟内,对于每一个一分钟的延迟,病人的存活的几率下降10%,该机构说。
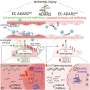
aed帮助通过发送一个电击通过传感器连接到心脏病人的胸部。冲击交付之前,传感器发送信息到电脑的AED找出电击是否会有所帮助。如果计算机决定,它将,一个语音提示告诉操作员要做什么,该研究所的网站上说。如果一切按计划进行,病人的心脏恢复跳动。
aed的问题是多种多样的。在一个案例中,一个去纤颤器由Defibtech被召回来解决软件问题可以取消的冲击。在另一起案件中,飞利浦医疗保健召回数千HeartStart单位因为错误的内存芯片是渲染设备不可操作。在另一个案例中,一个错误的组件促使召回aed由心脏科学。
这些问题是“预防和矫正”,据FDA公告。
“自动体外除颤器拯救生命,”威廉姆·迈希尔博士首席科学家FDA的设备和放射卫生中心在一份声明中说。“然而,该机构担心召回的数量和生产问题与这些设备,我们致力于与制造商来解决这些问题。”
虽然心脏除颤器的问题是严重的,FDA认为公众更好让他们在使用解决问题,而不是把他们完全退出市场。
拟议的规则来自该机构的循环系统设备面板。如果得到批准后90天的公众评论期,FDA计划18个月的“运动执法自由裁量权”,它说。
(c) 2013洛杉矶时报
由其特定信息服务