免疫细胞的职业道路
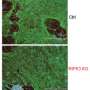
免疫系统产生的不同品种的T细胞(图1),如pathogen-destroying细胞毒性T细胞和免疫response-boosting辅助T细胞。调节性T (T注册)细胞抑制这些细胞,防止身体反应过度威胁或生成一个危险的自体免疫反应。
T注册细胞通常被转录调节蛋白Foxp3的表达,但新的工作领导的研究小组Shohei Hori过敏和免疫学研究中心的横滨证明这不是一个可靠的签名。
几组获得数据表明T注册细胞可以“转行”,失去Foxp3表达和转换到其他T细胞类型。许多发现和他的同事让他们提出另一种“异质性模型”。“我们的观察表明,这些现象可以完全解释为一个小“未提交”人口Foxp3 + T细胞没有假设重组,”他说。他的团队已经为这一假说提供了强有力的证据表明通过使用标签技术,允许他们目前细胞表达Foxp3区别于那些没有,但表达了这种蛋白质在过去。
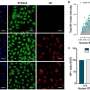
研究人员发现两组Foxp3-expressing细胞免疫刺激的反应不同。大多数表示这种蛋白质稳定在高水平,并表现出T的功能特征注册细胞。少数分数显示快速瞬变脉冲群Foxp3的表达,但最终发展成其他T细胞类型。这些“exFoxp3”T细胞似乎没有代表重新编程注册细胞,而是一个独立的T细胞,只有偶尔产生这种蛋白质。
有趣的是,他的团队也了解到一些T注册细胞进入一个状态,他们停止表达Foxp3,尽管他们保留的内存身份T注册细胞。这是实现通过化学修饰的DNA内Foxp3基因编码,和免疫刺激立即导致健壮的表达蛋白质。“这应该迫使人们重新考虑Foxp3的流行却过于简单化的观点主调节器(T)注册细胞,”霍里说。
确定这个表达式的事件概要因此可能更重要的是建立细胞身份比Foxp3的存在与否。“这是猜测,T注册家族是由高阶Foxp3的监管途径上游,但这个系统的本质是未知的,”Hori说。在未来的工作中,他计划与其他同事合作更密切的日本物理实验室调查这个问题。
更多信息:Miyao, T。,et al. Plasticity of Foxp3+ T cells reflects promiscuous Foxp3 expression in conventional T cells but not reprogramming of regulatory T cells.免疫力36岁,262 - 275 (2012)。
小松,N。,et al. Heterogeneity of natural Foxp3+ T cells: a committed regulatory T-cell lineage and an uncommitted minor population retaining plasticity.美国国家科学院院刊》上106年,1903 - 1908 (2009)。