部分肠道范围内设备可以中断病人
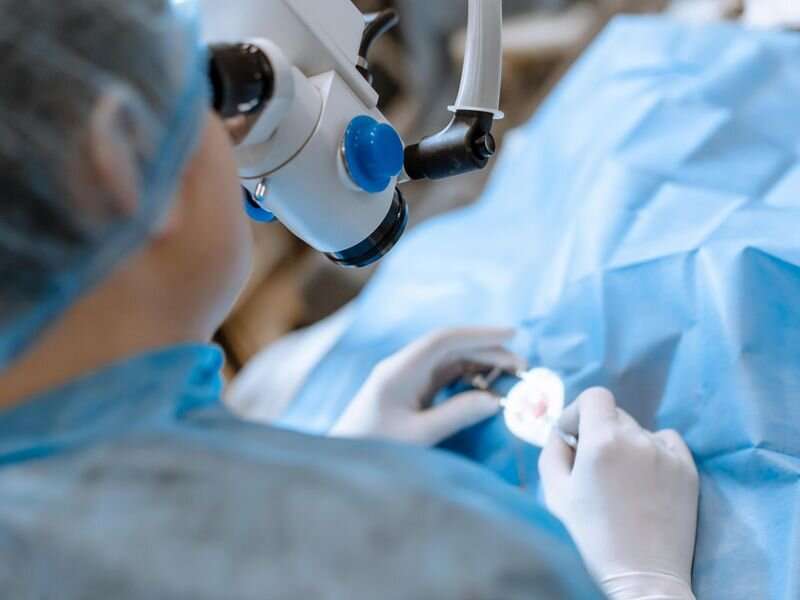
医疗器械用于诊断和治疗胰腺癌、胆管疾病越来越关注从美国食品和药物管理局在碎片掉落和仍在病人的身体。
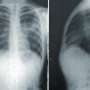
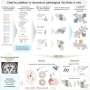
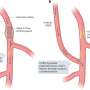
以前,FDA表示关注duodenoscopes因为他们很难清洁,可能传播细菌如大肠杆菌在患者身上。Duodenoscopes是灵活的,点燃的管螺纹的拿着相机通过口腔的胃和小肠(十二指肠)。
然而,当医院转向可支配技巧涵盖了相机和减少细菌传播,这已经导致了新的问题。这些由奥林巴斯医疗系统已经在病人的嘴和胃,据报告提交给FDA。
一些有锐利的边缘,导致内出血在病人,根据纽约时报。
FDA已经收到大约160投诉帽脱落。
“高于预期的数字类型的投诉,“据奥林巴斯的分析。
FDA发出了一个警告信在奥林巴斯公司后检查核电站在东京去年年底发现一次性部分为duodenoscopes和支气管镜吸阀,用于检查肺部,掺假或有缺陷的。
该机构表示,该公司的反应是“不足”,据《纽约时报》。
“FDA不同意风险足够低风险的病人不值得进一步的行动,”该机构说。
奥林巴斯发言人Jennifer Bannan表示,该公司已经采取措施来解决这个问题,“将进一步评估这些行动”和“扩大这些努力。”
“奥林巴斯非常重视这个警告信,”她在一份声明中说邮件的时间。“公司会尽全力在信中提出的问题及时。”
Duodenoscopes被用于在美国每年大约500000程序。
在投诉是一个从2021年5月,当一个医生报道软提示覆盖掉到病人的胃。
“这是决定允许通过胃肠道系统提示覆盖通过自然比进一步受到病人麻醉在试图删除它,”该报告称。
在另一项实验中,医生发现病人嘴巴流血后插入范围。范围被切除后,病人需要一个输血和痛苦的吞咽了天后。
而重复相同的过程之后,一位年长的范围没有可支配的提示,医生发现了一个治愈13-centimeter-long裂伤患者的食道。
虽然FDA中心的设备和放射卫生不建议取消或推迟程序“没有益处和风险的讨论”患者,该机构指出其他问题的工具可能表明不育问题。包括皱纹和气泡密封包装的一次性吸入支气管镜的阀门。
现在还不清楚医院和患者应该使用duodenoscopes可支配组件由其他公司或完全可支配duodenoscopes,纽约时报报道。
更多信息:全国胰腺基金会更多胰腺疾病。
版权©2023每日健康。保留所有权利。