研究人员发现现有药物可以破坏冠状病毒的复制
2020年初,埃里克·普林格尔(Eric Pringle)和布雷特·杜盖(Brett Duguay)发现自己大部分时间都在达尔塔珀大厦(Dal’s Tupper Building)七楼的微生物实验室里度过。病毒学家正忙于测试普通感冒冠状病毒的潜在抗病毒药物,并看到了有希望的结果。
两人都是博士后研究员,与克雷格·麦考密克(Craig McCormick)博士合作,他们正在研究一种已获批准的药物,这种药物已经被用于治疗癌症和肠易激综合症等其他疾病。他们的实验室最近完成了一项单独的研究,表明药物6-硫鸟嘌呤(6- tg)在实验室中抑制流感病毒复制方面惊人地有效。
然而,就在他们结束这项工作时,世界卫生组织宣布COVID-19为大流行,引发了广泛的封锁,实验室关闭,全球各地机构的一些研究中断。
一些研究高传染性和潜在致命的SARS-CoV-2和其他冠状病毒的研究人员除外。
Duguay博士在明亮、繁忙的实验室的餐厅里说:“那时我们决定,‘我们需要在冠状病毒上测试我们拥有的这种对抗流感的抗病毒药物。’”“所以,我们能够得到普通感冒冠状病毒,我们立即测试6-TG,它立即起作用。”
一个“惊人的结果”
Drs。杜盖和普林格尔以及麦考密克实验室的同事们于2020年3月获准回到他们的实验室,开始研究6-TG如何作用于普通感冒冠状病毒株,如OC43和229E。
和世界各地的科学家一样,他们也在试图了解,改变现有药物的用途是否可以安全有效地治疗COVID-19。他们很想了解更多关于冠状病毒如何与人类宿主细胞相互作用以及依赖性在哪里,这可能有助于确定它们的弱点在哪里。
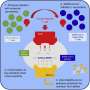
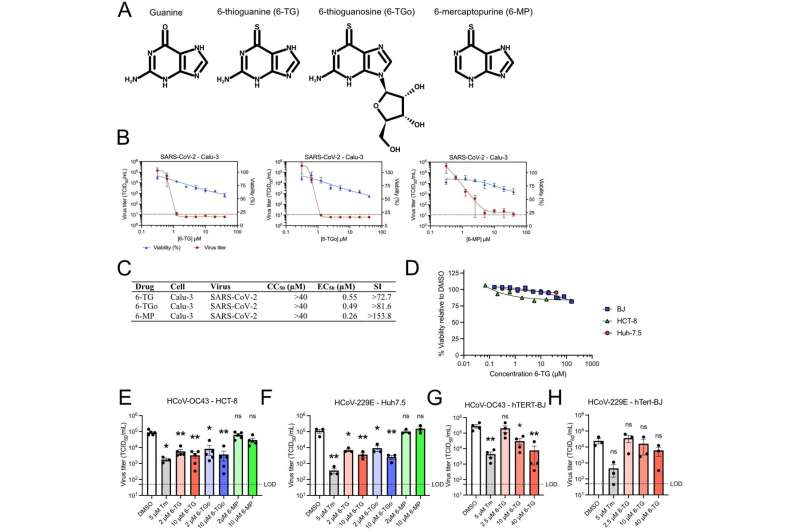
最终,他们发现了6-TG的一种新效应或作用机制。在细胞培养实验中,他们发现这种药物可以抑制包括SARS-CoV-2在内的人类冠状病毒的复制。它是通过干扰病毒的标志性刺突蛋白的发育来做到这一点的,刺突蛋白是穿透细胞膜所必需的宿主细胞并引发感染。没有它们,像SARS-CoV-2这样的病毒就不能与宿主细胞相互作用或传播。
“使用这种药物治疗的主要结果之一是它抑制了病毒制造大量刺突蛋白并将其合并到新的子代病毒或幼病毒中的能力,因此生成的幼病毒没有刺突,因此不能引发感染,”达尔学院微生物和免疫学系的病毒学家麦考密克博士说。
“这真是一个惊人的结果。”
普林格尔博士解释说,这些尖刺是糖基化的,这意味着它们被糖覆盖。这些糖通过保护刺突远离抗体,帮助病毒避开免疫系统。
他说:“我们发现抗病毒药6-TG抑制了适当的糖基化,所以刺突没有糖衣,不能正常工作。”
抑制病毒
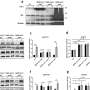
研究人员在最近的一篇论文中概述了他们的发现,他们使用了普通的感冒冠状病毒,他们在萨斯喀彻温省和卡尔加里大学的同事正在评估6-TG对SARS-CoV-2的影响。他们测量了被病毒感染的细胞和被药物治疗的细胞产生的病毒量。在处理过的细胞中复制的数量非常低。
Duguay博士说:“这就是你想要抗病毒药物做的事情——你想要它抑制病毒的生成量,这样病毒传播就不那么有效,生病的人就更少,生病的人就更少。”
该团队正在与达尔豪斯的药物化学家和神经学家苏丹·达尔维什博士合作,以更好地了解这种药物的工作原理,以及如何改进它以更有效地针对SARS-CoV-2。他正在进行计算研究,观察药物如何与细胞内的蛋白质相互作用。问题是药物对宿主细胞中的哪一种蛋白质起作用。
达维什博士说:“这可能就像大海捞针。”“我们想知道这些蛋白质中哪一种是导致癌症的罪魁祸首病毒以获取细胞,一旦我们找到蛋白质,我们就可以利用它计算方法看看我们是否能研制出比6-TG更好的药物。”
“我对此非常乐观药物."
研究人员强调,他们并不鼓励人们服用6-TG,而且迄今没有证据表明,因其他原因服用6-TG的人在治疗COVID-19方面有任何益处。这一发现是一个漫长过程中重要的第一步,该过程可能需要数年时间才能为未来的冠状病毒爆发产生治疗方法。
麦考密克博士说:“抗病毒药物在未来的病毒中扮演着真正的角色。”“让我兴奋的是,我们正在照亮一个新的领域,这可能是这类研究的一个新分支,我们提供的证据表明,这组人类蛋白质是很好的靶点,在病毒复制中发挥着重要作用。”
这项研究发表在PLOS病原体.