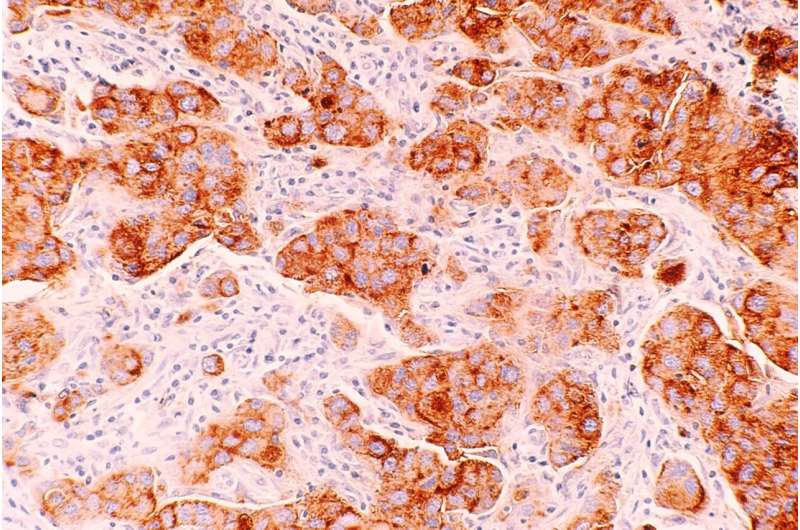
信贷:Unsplash / CC0公共领域
大约四分之一的复发性雌激素受体阳性乳腺癌(ER +)失去ER表达,这使他们对内分泌治疗,能够不受控制的生长。贝勒医学院的研究小组调查了这些细胞如何失去,和当前的研究发表在美国国家科学院院刊》上,他们揭示了一种机制,不仅解释了这个过程,而且提供了可能性来克服它。
“多年来,我们的目标是梳理出的复杂难题乳腺癌进展了解球员相互作用赋予抵抗治疗和持续增长,“说通讯作者Weei-Chin林博士,教授medicine-hematology和肿瘤的分子细胞生物学贝勒。“我们的目标是克服这个障碍恢复这些癌症的ER受体表达他们再次成为容易治疗,给患者更好的恢复的机会。”
乳腺癌细胞失去ER如何
两个细胞蛋白称为14-3-3τ和ERα36之前与乳腺癌的发展阻力内分泌治疗。
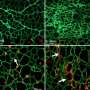
“使用人类乳腺癌ER +的小鼠模型,我们惊奇地发现,这些肿瘤中过度表达14-3-3τ导致所有的癌症细胞成为ER阴性(ER),”林说,丹邓肯L综合癌症中心的一员。“我仍然记得那一天我看到数据。的变化是显著毋庸肿瘤已经失去了呃。”
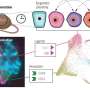
学习机制在动物模型是劳动密集型,耗时和昂贵的,所以研究人员开发了一个替代模式。学生第一作者Lidija a·威斯特Garan贝勒的癌症和细胞生物学研究生项目在林实验室工作,开发了一个球体模型模拟发展的人类乳腺癌细胞ER + ER和为未来的调查提供了一个非常有用的实验工具。
”乳腺肿瘤的病人,可以从ER + ER -年进展,在我们动物模型需要几个月但在我们的球体模型,它从ER +切换到ER -在1到2周,”Garan说。
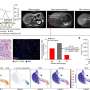
在实验室中球体模型研究小组发现,一旦14-3-3τvegf在肿瘤细胞在合适的条件下,细胞会增加水平ERα36这是紧随其后的是损失。
“其他分子的球员,比如AKT GATA3,也是必需的,“Garan说。“重要的是,我们还发现,产生的因素肿瘤微环境,包括成纤维细胞和免疫细胞的肿瘤与肿瘤细胞质量和相声,也必不可少的发展从ER + ER -。”
“我们知道14-3-3τERα36 AKT GATA3和所涉及的关键球员将ER +乳腺癌细胞呃——细胞。这里我们有决定他们如何功能相互作用,阐明道路的地图导致ER损失,”林说。“我非常激动,我们的球体乳腺癌模型我们现在有一个有价值的工具来研究不仅参与细胞的变化乳腺癌进展也来测试药物的能力抑制过程导致ER损失。”
“蛋白质14-3-3τ在乳腺癌的60%左右。不是所有的病人都有高14-3-3τ会失去,但是对于那些做的,我们的发现可能有一天帮助恢复他们的肿瘤therapy-sensitive状态,”Garan说。“转化方面的研究一直是接近我的心带来发现诊所和改善人们的生活。”
杨小贝勒医学院也是一个作家的工作。
更多信息:Lidija a·威斯特Garan et al, 14-3-3τ驱动器通过雌激素受体损失ERα36感应和GATA3抑制乳腺癌,美国国家科学院院刊》上(2022)。DOI: 10.1073 / pnas.220921111。www.pnas.org/doi/10.1073/pnas.2209211119
期刊信息:美国国家科学院院刊》上
所提供的贝勒大学医学院