Nanofiber-based可生物降解millirobot可以释放药物在肠道靶向位置
nanofiber-based可生物降解millirobot叫做Fibot成功开发的研究学者为首的香港城市大学(城大)。Fibot肠道内可以移动并降低环境的酸碱度,从而释放不同的药物在不同的固定位置。研究揭示millirobots的发展,与控制释放药物的潜在应用在肠道靶向位置。可生物降解的研究也促进了发展和自适应设备与生物医学应用。
沈Yajing博士领导的研究小组是在城大的生物医学工程系副教授(BME)。他们的研究结果发表在学术期刊事名为“Nanofiber-based可生物降解millirobot可控锚固和自适应逐步释放功能。”
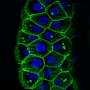
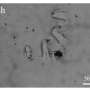
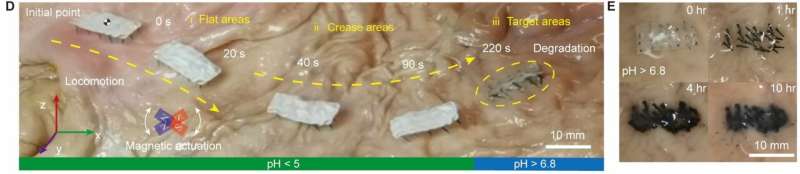
Fibot可以移动和“锚定”在肠道,由外部磁场驱动的
有针对性的药物释放在胃肠道中的位置是很困难的,由于胃和肠道的酸/碱环境,以及胃壁的粗糙表面,和小肠的蠕动。然而,沈博士和他的团队克服了这些障碍。
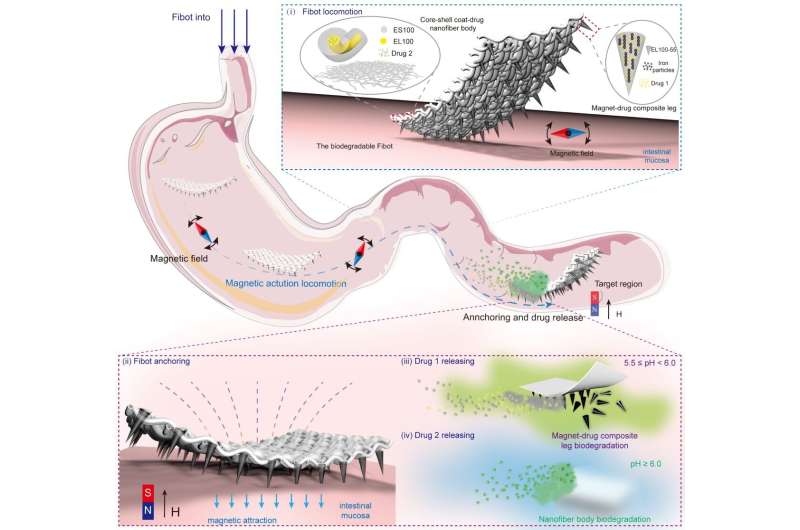
“我们命名这个nanofiber-based软millirobot Fibot。它可以用于可控锚固和完全可降解以应对周边环境的pH值。因此,Fibot可以各种药物嵌在它的身体和释放腿一步一步在胃肠道,”沈博士说,他介绍了团队的研究成果。
“锚定”意味着Fibot可以呆在一个固定的位置搬到所需的位置后在肠道内,没有被蠕动推开。由一个外部磁场,类似Fibot可以有效地在复杂环境中移动的胃肠道和锚本身肠壁通过应用一个强大的磁场。
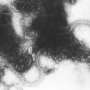
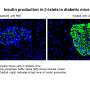
在兔子体内实验证明Fibot能够完全降解四个小时
“Fibot的腿可以穿透肠粘膜,使它锚定在所需的小肠位置没有被蠕动推开。这是一个药物释放在目标位置的先决条件。同时,精确控制的磁场,Fibot的腿不到达的外层黏膜下层和肌层胃肠道,从而有效地避免肠穿孔的潜在风险,”沈博士解释道。
用Fibot团队进行各种实验。他们发现,由磁力驱动,Fibot搬到7厘米10秒猪的胃,这是崎岖的,湿和酸性,pH值为5。这证明Fibot机车在胃里的能力。
该小组还进行了体内实验与Fibot兔子的肠。当Fibot搬到目标肠道地区,团队更强的磁场应用于锚肠道组织。Fibot在那里呆了四个小时,最终完全退化在那个位置。
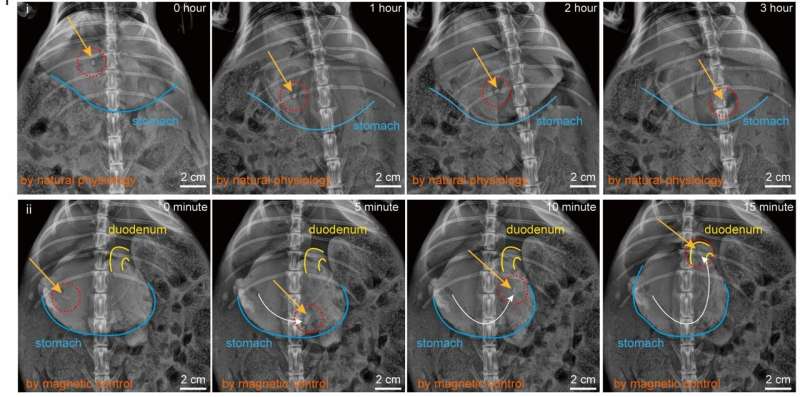
制作材料的不同pH-responsive降解能力使可控药物释放
Fibot的另一个特点是它能够释放药物。关键在于制造材料。团队装配式Fibot nanofiber-based软膜体和类似数组分开可生物降解材料,然后组装的两部分磁field-assisted电纺的方法。
特殊的核壳结构纳米纤维用于身体结构使药物封装在外壳内。捏造针状的腿时,团队调整材料的成分,和里面的药物被放置。
“因为我们调整了材料在制造、Fibot的身体和腿可以在不同的pH值降低,允许我们控制逐步释放不同的药物封装在Fibot的身体和腿,“沈博士补充说。
实验表明,在酸性环境中那样在胃里,在pH值小于或等于5,Fibot结构保持稳定,无渗漏的封装药物。当Fibot位于一个环境pH值大于或等于5.5,身体仍然保持不变,但腿慢慢溶解,释放嵌入式药物逐渐约40分钟。剩下的身体仍然可以感动磁力。在一个环境pH值大于6,其余身体7个小时之内完全降解,释放另一种药物在体内的封装。
Fibot完全是生物相容性和安全的生物医学使用
“体内实验证明,Fibot完全是生物相容性和生物可降解的,因此它不会引起任何肠梗阻。锚定到肠组织并没有导致任何炎症反应,所以我们相信Fibot生物医学使用是安全的,”沈博士补充说。
Fibot揭示了功能性millirobot设计是完全生物降解和可以释放药物逐步在一个固定的位置。发现潜在的用于未来生物医学治疗,如目标地区交付和可编程的释放,为临床应用和肠道高分子交付。“Fibot局部治疗和有潜力提供了一个新的解决方案为大分子皮肤药物释放,“沈博士总结道。
更多信息:荣Tan et al, Nanofiber-based可生物降解millirobot可控锚固和自适应逐步释放功能,事(2022)。DOI: 10.1016 / j.matt.2022.01.023