这一发现指向了帕金森病的可能病因
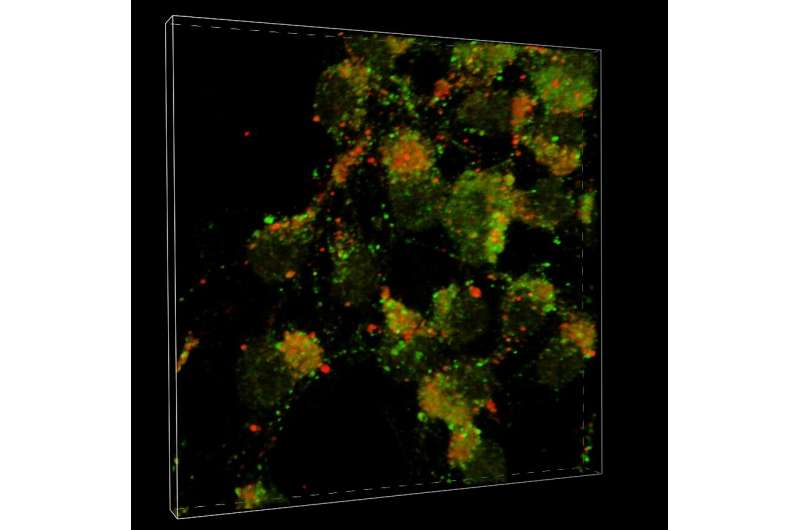
根据斯克里普斯研究所科学家的一项新研究,帕金森病可能在一定程度上是由细胞压力相关的生化事件引起的,这些事件破坏了关键的细胞清理系统,导致有害蛋白质聚集物在大脑中扩散。
这一发现发表在神经科学杂志这项研究将于2022年2月发布,提供了一个关于帕金森病进展的清晰且可验证的假设,并可能导致能够显著减缓甚至停止帕金森病的治疗方法。
“我们认为,我们关于这种明显的疾病驱动过程的发现对于开发能够特异性抑制疾病在大脑中传播过程的化合物非常重要,”该研究的资深作者斯图尔特·利普顿(Stuart Lipton)说,他是医学博士、阶梯家族捐赠主席、神经退行性疾病新药中心创始联合主任、斯克里普斯研究所分子医学系教授。
帕金森氏症影响着美国大约100万人。它的确切触发因素尚不清楚,但它会导致神经元在关键大脑区域以特定顺序死亡。中脑中一小组产生多巴胺的神经元被杀死,就会导致典型的帕金森氏震颤和其他运动障碍。对大脑其他区域的伤害会导致各种其他疾病的症状,包括帕金森病晚期的痴呆症。一种与痴呆症密切相关的综合征,在疾病病程早期发生,被称为路易体痴呆(LBD),在美国约有140万人受到影响
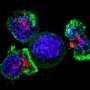
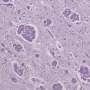
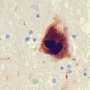
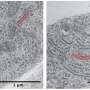
在这两种疾病中,受影响的神经元含有异常的蛋白质聚集,称为路易体,其主要成分是一种叫做突触核蛋白的蛋白质。先前的研究表明,在帕金森氏症和LBD中,α -突触核蛋白聚集物可以从一个神经元扩散到另一个神经元,显然是通过大脑传播疾病过程。但是,α -突触核蛋白聚集物是如何以这种方式形成和扩散的,目前尚不清楚。
Lipton的实验室和其他研究人员在之前的研究中发现的一条线索是,帕金森/LBD疾病过程会产生高活性的含氮分子,包括一氧化氮。原则上,这些活性氮分子可以破坏重要的细胞系统,包括通常控制蛋白质聚集的“管家”系统。
在这项新研究中,斯克里普斯研究小组证明了这一想法的有效性,他们展示了一种名为s -亚硝基化的氮分子反应可以影响一种名为p62的重要细胞蛋白,引发α -突触核蛋白聚集物的积聚和扩散。
p62蛋白通常有助于自噬,这是一种废物管理系统,帮助细胞摆脱潜在有害的蛋白质聚集物。研究人员发现证据表明,在帕金森病的细胞和动物模型中,p62在受影响的神经元中以异常高的水平被s -亚硝基化。这种p62的改变抑制了自噬,导致α -突触核蛋白聚集物的积聚。聚集物的积累反过来导致受影响的神经元分泌聚集物,其中一些聚集物被附近的神经元所吸收。
“我们观察到的过程似乎与帕金森氏症和LBD的大脑非常相似,”该研究的第一作者、利普顿实验室的工作人员吴昌基博士说。
研究人员还测试了LBD患者死后的大脑,再次发现在受影响的大脑区域,s -亚硝基化p62的水平异常高,这支持了这一过程发生在人类身上的观点。
Lipton和Oh说,蛋白质的s -亚硝基化在细胞应激的许多情况下变得更有可能,包括蛋白质聚集物的存在。因此,p62的这种化学修饰可能是自我强化过程中的一个关键因素,这个过程不仅使脑细胞的压力超出了它们的极限,而且还将压力的来源传播到其他脑细胞。
该团队目前正致力于开发专门抑制p62 s -亚硝基化的类药物化合物。尽管开发这种化合物作为潜在的商业药物还需要数年时间,但原则上,它们可以减缓帕金森/LBD疾病的进程或防止其在美国的进一步传播大脑在它开始之后,利普顿说。
进一步探索