面对抗生素耐药性,“我们已经没有选择了”

专家预测,如果不采取干预措施,到2050年,耐多药细菌感染问题可能是灾难性的,每年造成近1000万人死亡。
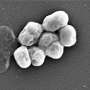
为了寻求解决方案,美国国立卫生研究院(National Institutes of Health)向德克萨斯大学阿灵顿分校(University of Texas at Arlington)生物学助理教授约瑟夫·博尔(Joseph Boll)授予了一项为期五年、价值180万美元的赠款,以识别和抑制鲍曼不动杆菌(Acinetobacter baumannii)的防御机制,鲍曼不动杆菌是一种在医院和临床环境中猖獗的病原体。
鲍曼氏弧菌会引起血液感染,尿路还有肺部,或者身体其他部位的伤口。感染通常用抗生素治疗,但许多菌株对药物有耐药性,包括碳青霉烯类药物有效的抗生素通常用于严重的耐多药细菌感染。
Boll说:“在之前的研究中,我们发现当鲍曼拟单胞菌经历压力时,比如抗生素治疗,它会修改其细胞包膜,以在较长时间内耐受抗生素。”“特定的修饰可以让细菌存活足够长的时间,从而获得真正的抗生素耐药性,这可能导致抗生素治疗失败。这可能发生在接触抗生素的24小时内。”
Boll的团队希望能够确定在抗生素存在的情况下,细胞包膜中的哪些适应性使病原体能够存活,以及存活如何有助于获得真正的耐药性。
最近发表在该杂志上的一项题为“间隔a类青霉素结合蛋白活性和ld转肽酶介导耐粘菌素低脂糖缺陷鲍曼不动杆菌的选择”的研究mBio研究小组发现,两种ld转肽酶能重塑鲍曼假单胞菌的细胞包膜,以促进其在压力下的生存,比如在抗生素治疗期间经历的那种压力。
有了这一突破,生物学和微生物学双学位的大四学生汉娜·博弗曼(Hannah Bovermann)正在解剖编码细菌的ld转肽酶的基因,以了解是什么压力条件诱发了它们的激活。她分离出了ld -转肽酶启动子,这是DNA中控制其他DNA部分何时被使用的部分,并将其粘合到另一个基因上,该基因的功能是将细菌细胞变成蓝色。当细胞处于想要修改细胞包膜以保护自己的环境时,它就会变成蓝色,Bovermann可以观察到这种变化的时间。
为了引起这种反应,她使用抗生素,在不同的温度变化下进行实验,将细胞暴露在pH梯度中,并使细胞处于营养匮乏状态。
Bovermann说:“每一次反应都让我们更接近于理解细胞包膜的改变是如何在压力下保持细菌细胞完整的。”
研究人员希望在细胞表面找到新的靶点抗生素从而加强现有药物对抗鲍曼弧菌感染的效力。
耐药细菌已经走投无路卫生保健提供者Boll说,使用组合疗法,即使用多种药物来治疗细菌感染,但即使是这些方法也变得越来越无效。
“这已经变成了一场游戏。研究人员发现了一种新的抗菌素,然后细菌对它产生了抗药性。我们已经没有选择了。”“细菌耐药性的发展速度很快就超过了新抗生素的发展速度。”
更多信息:Katie N. Kang等,A类青霉素结合蛋白活性和ld转肽酶介导耐粘菌素低脂糖缺陷鲍曼不动杆菌的选择,mBio(2021)。DOI: 10.1128 / mBio.02185-20