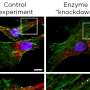
对接肽,缓慢锁定,打开治疗阿尔茨海默病的可能途径
阿尔茨海默病的治疗进展缓慢得令人沮丧。休斯顿的一组科学家认为,小范围的挫折可能会导致一种新的治疗途径。
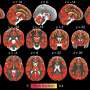
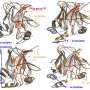
休斯顿大学(UH)和莱斯大学(Rice University)与莱斯理论生物物理中心(CTBP)的研究人员通过实验和计算发现,淀粉样β肽,小分子它们在大脑中丰富,经历了几个中间阶段的挫折,因为它们“停靠并锁定”到不断生长的原纤维的尖端。
折叠蛋白质倾向于寻找最简单的方法来达到它们的功能形式。同样的,淀粉样肽寻找最简单的方法来结合生长中的纤维的尖端,但有时会受阻——当原子之间的正负力没有立即对齐时。
当它们最终对齐时,不断增长的原纤维形成了与阿尔茨海默病和其他神经系统疾病有关的胶质斑块。最新研究表明美国国家科学院院刊这表明可以开发药物来利用肽的中间状态来稳定原纤维Tips和block进一步聚合。
哈佛大学化学和生物分子工程师彼得·维基洛夫说,在他的实验室里观察β淀粉样蛋白原纤维的生长并不是一件难事。他说:“以前用原子力显微镜观察纤维蛋白的研究集中在更奇特的行为上,因为具有稳定增长速度的淀粉样蛋白原纤维有点无聊。”
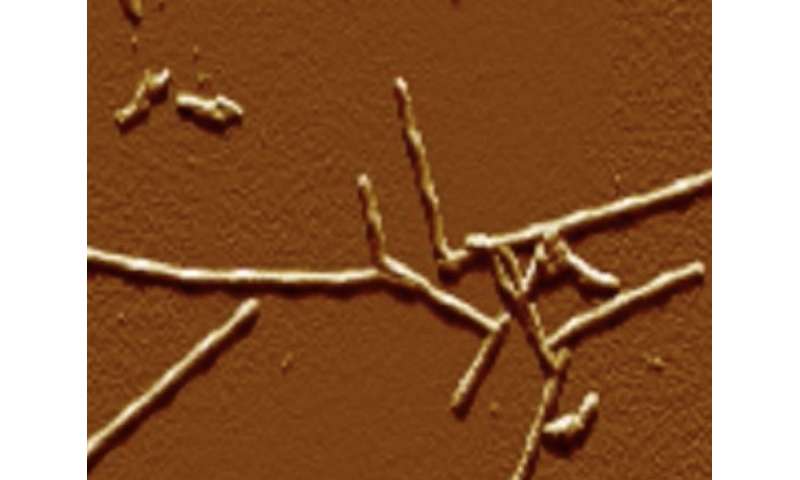
“但我很着迷,因为生长速度与溶液中多肽浓度的相关性承载了大量的信息,”vekilv说。“它有助于测量速率常数,这是一个容易建模的量。”
他说,莱斯大学物理学家彼得·沃利斯(Peter Wolynes)的实验室专门建立蛋白质和染色体折叠的计算机模型,他建议用尿素来破坏稳定的生长,尿素可以使蛋白质变性(或展开),这可能为淀粉样原纤维的形成提供有用的数据。的确如此。
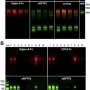
“一件奇怪的事情发生了,”vekilv说。尿素使原纤维不那么稳定,这意味着原纤维中分子之间的键变得不那么牢固。但这也让它们长得更快。这是一个非常严重的矛盾,违背了化学的经验法则。
“但有经验法则,也有基本法则,”他说。“我们想,这是在试图告诉我们一些事情。”
进一步的实验表明尿素“破坏了错误的肽键的稳定,”Vekilov说。“它使纤维生长得更快,但也向我们展示了中间受挫的步骤。最重要的是,我们现在有证据表明,在原纤维的末端有一冠状紊乱的肽链试图对接和锁定,这些都是药物靶点。
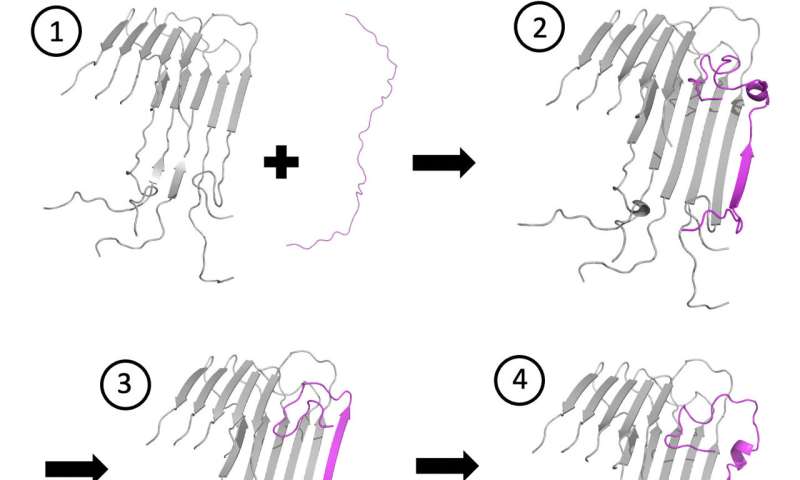
他说:“封锁每一种肽是不合理的,因为它们的数量可能是纤维尖端的10万倍。”“我们发现的美妙之处在于,纤维尖端是纤维化的阿喀琉斯之踵,我们所要做的就是阻断尖端的复合体。”
Wolynes注意到有沮丧的迹象早期的研究在纤维聚集中发现了连接的证据。他说:“实验中出现了两件事。”“一是人们用于β淀粉样蛋白生长的几乎所有动力学模型都太简单了。这并不意外。另一个是变性改变了平衡,它也可以改变折叠的速率从而告诉你跃迁态出现的位置。
Wolynes说:“在早期关于纤维成核的论文中,我们注意到,似乎有一些奇怪的过程,蛋白质必须从过渡状态返回。”“所以彼得就去调查了,我认为他是第一个这样做的人。”
他说,有一种方法可以阻止原纤维的生长,这可能有助于解决科学家之间长期存在的分歧,即原纤维是会导致神经系统疾病,还是会保护大脑免受其他怀疑,尤其是纠结的怀疑τ蛋白.
“我们的想法是在顶端下毒,让它无法生长,而不是破坏整个纤维的稳定,”Wolynes补充道。“当然,这引起了关于原纤维是好是坏的大争论。”
计算模型可能表明,阻止原纤维既可以阻止阿尔茨海默病的影响,也可以使其恶化。不管怎样,Wolynes说科学家将会有一个更明确的答案。
“在我看来,有趣的是提供了一个新的目标,我们将探索一些可能改变尖端性质的药物,”他说。“无论如何,这些分子将提供有趣的工具来理解纤维生长是如何发生的。”
哈佛大学的研究生Yuechuan (Alex) Xu和莱斯大学的Kaitlin Knapp是这篇论文的共同主要作者。共同作者是莱斯大学博士后研究员尼古拉斯·谢弗和客座教员阿拉姆·达蒂安;哈佛大学校友Mohammad Safari,现在是普林斯顿大学博士后研究员;凯尔·勒(Kyle Le),哈佛大学校友,前莱斯大学研究实习生。vekilv是John and Rebecca Moores化学和生物分子工程教授,也是UH的化学教授。Wolynes是D.R. Bullard-Welch基金会的科学教授,化学、生物科学、物理学和天文学教授,CTBP的联合主任。
进一步探索