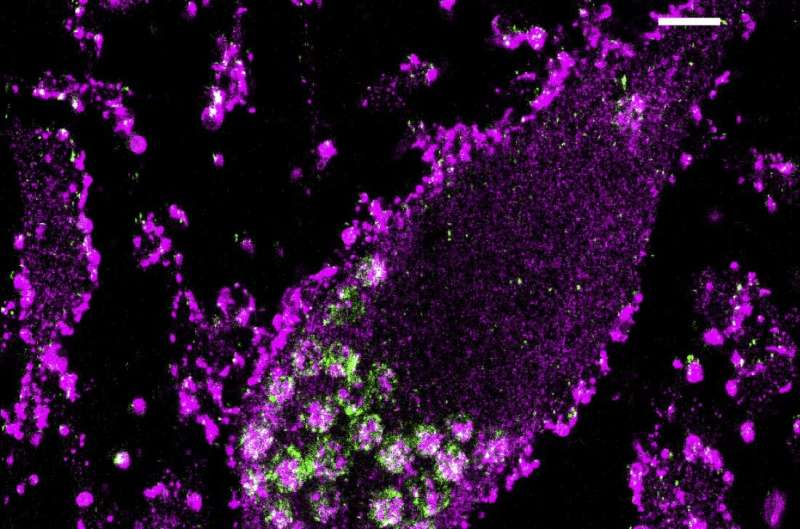
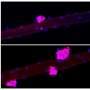
神经元的超分辨率显微镜显示脂质在抑制蛋白酶基因的溶酶体中的积累。信用:UCSF.
当细胞中的单个基因导通或关闭时,其产生的存在或不存在会影响细胞的功能和存活。在一个新的研究中出现了5月24日自然神经科学,UCSF研究人员通过分别在人类基因组中分别切换每个20,000个基因来成功在人神经元中成功编目了这种影响。
在这样做时,他们已经创建了一种可以用于许多不同的小区类型的技术,以及使用新技术的其他研究人员可以贡献类似的知识,在整个范围内创造疾病中基因功能的图片人体细胞。
“这是揭开后面机制的关键下一步疾病基因“神经变性疾病和UCSF威尔省神经科学研究所副教授博士教授”博士·坎普曼,博士议员说,“神经科学研究所副教授说明了该工作利用基因测序,干细胞技术和CRISPR的近期进步。
“链接有很多人类遗传学研究特定基因“克汉曼说,”我们正在做的工作可以了解这些工作基因导致疾病,让我们瞄准治疗。“
他的团队对精确定位可能参与的基因感兴趣神经退行性疾病如阿尔茨海默氏症和相关形式的痴呆。它们的方法包括使用干细胞生成的人神经元并确定当单个基因打开和关闭时细胞中发生的化学变化。
它们特别是在细胞中产生氧化应激的基因表达的下游变化,这是高反应性氧的情况可以产生毒性环境。这种病症被认为有助于神经变性。
翻转基因交换机显示出意外结果
为了调查个别基因并了解更多关于他们的职能,Kampmann采用了一种称为CRISPR激活/干扰,或CRISPR A / I的技术,他作为jonathan Weissman,博士学位癌细胞上工作的UCSF后博士学位学者。。,前UCSF教职员和当前的白头研究所会员和调查员与霍华德休斯医学院。CRISPR A /我允许研究人员暂时转动单一基因关闭或接通,看看如何改变会影响其他基因的表达。
使用该工具在人神经元上,昆曼曼在另一个接通和关闭后转基因,使用染料来可视化高反应性氧的存在。在他的研究结果中最有趣的是,切断蛋白质的基因,这些蛋白质是蛋白酶,通常有助于细胞对废物的再循环,大大增加了氧化胁迫的水平。
在神经元中,Praposin与称为溶酶体的一部分细胞有关,其中生物分子和毒素以各种方式分类并释放。“乍一看,雷帕莫辛应该与氧化分子无关。它引起了我们的注意,因为这种基因最近与帕金森病联系起来,”克兰克曼说。“真正令人兴奋的是,现在,随着这种Crispr屏幕的结果,我们有一个基于细胞的模型,以帮助我们了解落后的联系。”
然后,团队开始探讨昆曼恩称之为“侦探故事”,以了解缺乏肺炎蛋白酶与神经变性相关。研究人员发现,基因的抑制导致了一种称为年龄颜料的物质的堆积,这在老化细胞中已经看到,其溶酶体不再有效降低材料。研究人员发现,年龄颜料被捕获的铁,产生触发硬化的反应性氧分子,依赖于细胞死亡的铁依赖性过程。
“通过简单地失活,”Kampmann说,“在只有几天中,我们可以产生通常花在人体中发展的老化的标志。”
构建基因功能的全局数据库
Kampmann的遗传屏幕是对人类神经元进行的第一个。
他观察到的级联的改变是特异性的神经元的功能,并且与一系列条件有关。他表示,结果为使用CRISPR A / I进行了类似屏幕的结果,寻找促进神经元和其他类型的不同细胞中其他类型的疾病相关环境的变化。
为此,Kampmann创建了一个名为Crisprbrain的开放式访问数据库,其中他和其他科学家可以分享和研究大规模数据集,如由他的基因屏幕生成的大规模数据集。然后,应用更高级的计算技术,如机器学习,然后可以检测到这种数据海洋中的模式。
“通过从许多不同的实验室和不同疾病背景下成为许多不同细胞类型的屏幕的数据公约,我们可以达到批评的信息,”他说。“汇总和交叉分析所有这些都有巨大的力量。”
该团队的下一步是在由已知患者源自患者的干细胞制成的神经元上进行类似的筛网,以及看其他细胞如在脑病中发挥作用的星形胶质细胞和微胶质细胞。
Kampmann的希望是技术和数据库被广泛采用。“现在我们可以以系统的方式做到这一点,我们可以真正解释基因如何为疾病有助于治疗这些条件的潜在过程。”
更多信息:基因组 - 宽/屏幕在人神经元中的筛网将溶酶体失败与硬化,自然神经科学(2021)。DOI:10.1038 / S41593-021-00862-0
信息信息:自然神经科学
由...提供加州大学旧金山