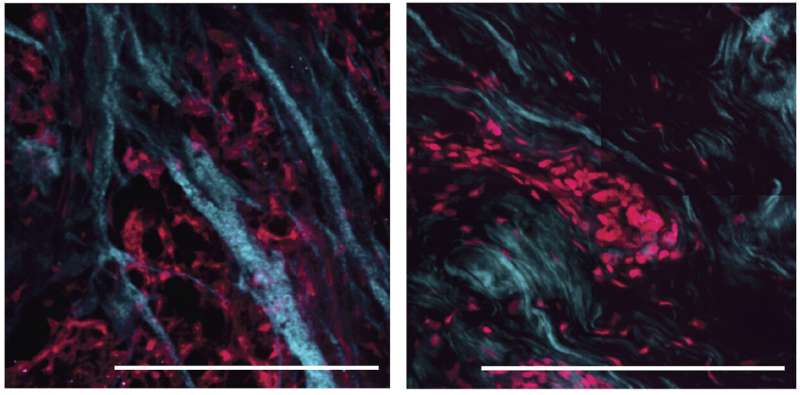
与未经处理的乳腺肿瘤(左)相比,在治疗(右)后在残留肿瘤中重组细胞外胶原基质(蓝色),激活肿瘤细胞(洋红色)中的信号通路,其允许它们存活并引发肿瘤复发。信用:©2021排水管等。最初发表在实验医学杂志。DOI: 10.1084 / jem.20191360
加州大学旧金山分校(University of California, San Francisco)的研究人员发现,侵袭性三阴性乳腺癌(tnbc)可以通过重组和软化癌细胞周围的胶原基质来逃避治疗。这项研究将于4月2日发表在实验医学杂志(杰姆),表明较软的基质激活促进癌细胞生存的信号通路,并表明靶向该途径可以提高化学和放射疗法在TNBC患者中的有效性。
TNBC是一种侵略性的乳腺癌,具有比其他形式的疾病的存活率更差。由于TNBC细胞缺乏HER2信号传导受体和雌激素和孕激素激素受体,因此不能通过特异性靶向这些蛋白质的药物来消除它们。相反,TNBC患者通常用手术和化疗/辐射的组合治疗,但这些治疗通常无法完全消除肿瘤,导致局部复发和转移到其他组织。
“目前,没有可靠的方法来识别可能会良好的患者,并且那些可能抵抗治疗的患者,”企业生物工程和组织再生中心教授和主任UCSF的手术。“迫切需要更深入地了解TNBC在TNBC中的治疗反应生物学基础,将提供通知治疗决策和发展有效策略的克服治疗耐药性。"
影响治疗反应的一个因素是肿瘤内癌细胞周围的胶原蛋白和其他蛋白质的网状结构。这种细胞外基质可以激活细胞内的各种信号通路,从而决定细胞在受到压力时是否会死亡。
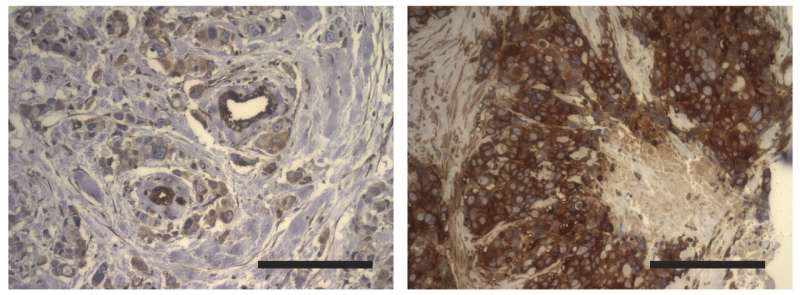
与未经治疗的乳腺肿瘤(左图)相比,治疗后残余肿瘤(右图)中NF-κB(棕色)由于细胞外基质软化而升高。NF-κB促进癌细胞的生存和随后的肿瘤复发。排水等人。最初发表在实验医学杂志。DOI: 10.1084 / jem.20191360
韦弗和同事,包括凯瑟琳C.公园,UCSF的放射肿瘤科教授和主席,以及研究生艾里森P.流失,分析了来自TNBC患者的肿瘤样品中的细胞外基质。在未处理的TNBC中,将胶原蛋白蛋白排列成长,直链纤维,产生比正常健康的乳腺组织更硬的基质。但在用化疗治疗的TNBC中,剩余肿瘤中的胶原纤维被重新组织以形成较软的基质。
“这提出了一种有趣的可能性,即软化的、重塑的细胞外基质可能与耐治疗的残余肿瘤组织的发病机制有因果关系,”韦弗说。
研究人员发现,当在较软的时,实验室或小鼠中生长的肿瘤或小鼠的肿瘤更耐辐射和化疗剂紫杉醇细胞外基质。在坚硬环境中生长的癌细胞会激活一种被称为JNK的信号蛋白,这种蛋白使癌细胞在应激时更容易死亡。相比之下,癌细胞被一个更温和的矩阵激活一种名为NF-kB的蛋白质,它可以抵消JNK,促进细胞存活。因此,用抑制NF-kB的药物治疗小鼠可以改善其治疗反应,与放疗联合时显著减缓肿瘤生长。
韦弗和同事发现,TNBC患者肿瘤具有高水平的NF-KB活性显示出较高的治疗率。NF-KB活性也升高,在处理后留下的重新渗透,软化肿瘤。
“设计用于调节刚度的NF-κB或JNK活动的疗法可能改善TNBCS的治疗响应,并提高这些患者的长期存活,”韦弗说。“然而,需要进一步的努力来澄清介导治疗抵抗和发展有效,选择性和安全治疗的机制的性质。”
更多信息:等2021年。j . Exp。地中海。rupress.org/jem/article-lookup ... /10.1084/jem.2019360
期刊信息:实验医学杂志
由...提供洛克菲勒大学出版社