α射线导弹疗法:肿瘤细胞攻击来自细胞内的地区
一个特异的l型氨基酸转运蛋白1 (LAT1)是癌症组织中高度表达。抑制的功能LAT1已知有抗肿瘤作用,但有有限的进步发展的代理商针对LAT1放射性核素治疗。现在,大阪大学的一个多学科的研究小组建立了一个有针对性的新药物瞄准LAT1 alpha-therapy。
研究人员首先产生α射线发射器211年砹,不容易砹(At)是地球上最稀有的天然元素。针对alpha-therapy选择性提供α-emitters肿瘤;优于传统β-therapyα衰变是具有高度针对性和高线性能量转移引起DNA双链断裂,有效地引起细胞死亡。短的半衰期和有限的组织渗透的阿尔法辐射确保高疗效与周围一些副作用正常细胞。
接下来,将放射性同位素癌症细胞,研究人员将它连接到α-Methyl-L-tyrosine LAT1高亲和力。这种托词利用高营养需求的迅速增殖的癌细胞。
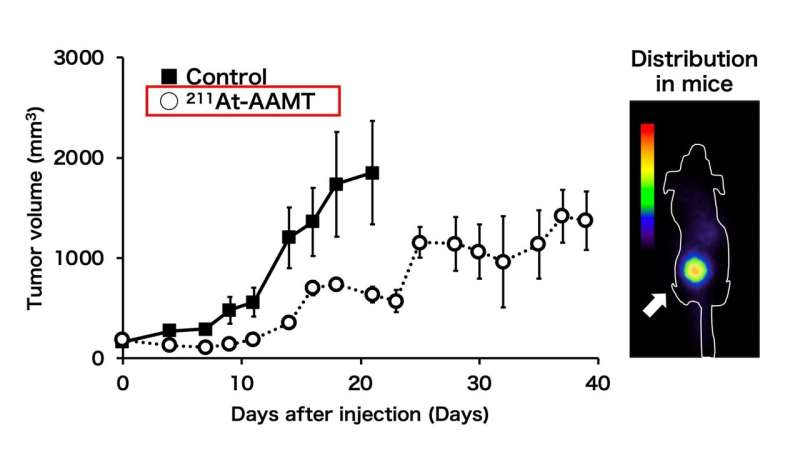
“我们发现,211年At-labeledα-methyl-L-tyrosine (211年At-AAMT)高亲和力LAT1、抑制肿瘤细胞和体外DNA双链断裂引起的,”报告Kaneda-Nakashima合子副教授,第一作者。“扩展我们的研究中,我们评估的积累211年At-AAMT和LAT1在实验小鼠模型的作用。进一步的调查显示,在人类胰腺癌细胞线211年At-AAMT选择性积累在肿瘤和抑制增长。在更高的剂量,它甚至抑制转移的肺转移性黑色素瘤小鼠模型”。
-
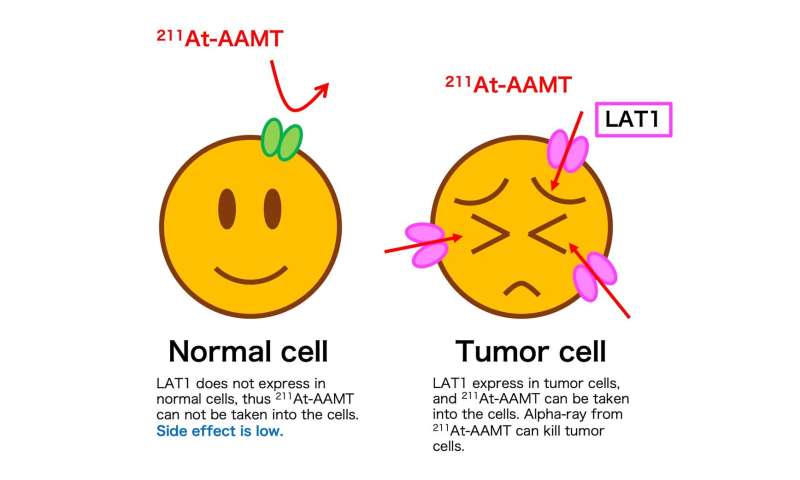
图2:机制211年通过LAT1 At-AAMT癌症细胞。信贷:大阪大学 -

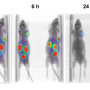
图3:肿瘤转移抑制通过211年使用B16F10 At-AAMT模型。实验小鼠肺的照片。信贷:大阪大学
教授Atsushi筱原资深作者,解释说:“我们可以建立的功效211年砹治疗癌症包括先进和转移性恶性肿瘤,以及氨基酸转运蛋白的效用LAT1放射性核素治疗的工具。交付的药物是癌症,可以从细胞内攻击后被作为营养。”
增加功效是计量方便。作为一个注射短程放射药剂,211年At-AAMT可能在门诊管理,在传统辐射协议一个巨大的优势,甚至可能是另一个在特定癌症手术。这种方法有巨大的潜力不仅彻底改变放射性核素治疗胰腺癌癌症但其他恶性肿瘤缺乏有效的治疗包括晚期或转移性疾病。
更多信息:金田从轻量中岛美嘉等人α量排放211年癌症治疗使用高AAMT瞄准LAT1癌症科学(2020)。DOI: 10.1111 / cas.14761