细胞质交通堵塞破坏了睡眠-觉醒周期
佛罗里达州立大学的Kaist数学家及其合作者已经确定了痴呆症和肥胖等衰老和疾病如何引起睡眠障碍的原则。数学建模和实验的组合表明,由衰老,痴呆和/或肥胖引起的细胞质充血扰乱了人体中的昼夜节律,并导致不规则的睡眠唤醒周期。这一发现表明,用于解决不稳定睡眠唤醒周期的新处理策略。
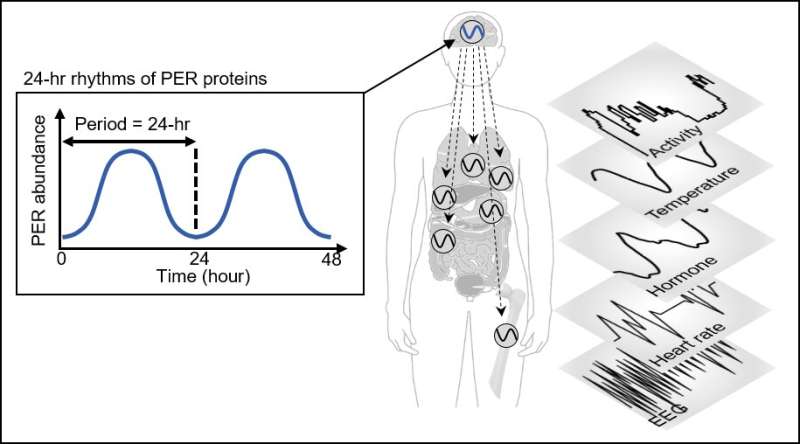
人体是根据“昼夜节律”来调整睡眠时间的,而昼夜节律是由我们的时间控制系统“生物钟”调节的。生物钟这个时钟通过一种叫做PERIOD (PER)的蛋白质产生24小时节律,告诉我们的身体什么时候休息(见图1)。
PER蛋白的含量在半天内增加,然后在剩下的半天内减少。其原理是在细胞质中积累数小时的PER蛋白进入细胞核从而阻碍了PER基因的转录,从而减少了PER的数量。
然而,它仍然是一个谜团,每分子数千人可以同时进入核在一个复杂的细胞环境中,其中各种材料共存并且可以干扰每种材料。这就像在纽约城市的数千名员工寻找一路,每天同时进入办公大楼。
来自Kaist Mathemical Sciences教授Jae Kyoung Kim教授领导的研究人员通过开发一种时尚和概率模型来解决了谜团,该模型描述了细胞环境中每分子的运动。
这项研究是与佛罗里达州立大学的chogon Lee教授的团队合作进行的,实验是在佛罗里达州立大学进行的,结果发表在《科学》杂志上美国国家科学院院刊(pnas.) 上个月。
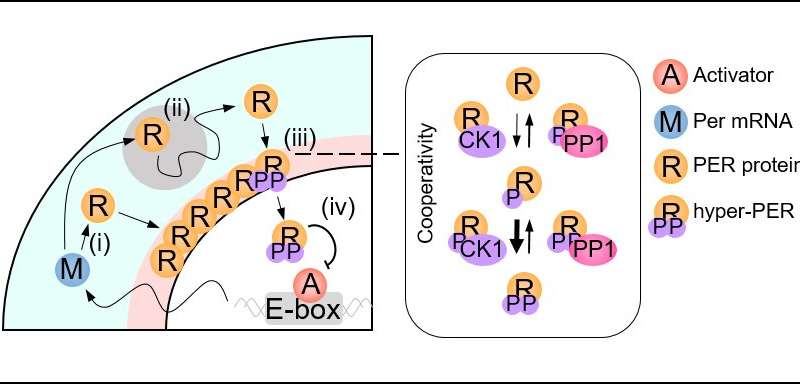
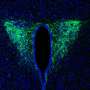
联合研究团队的空间随机模型(见图2)描述了每分子的运动细胞证明了PER分子应充分凝聚在细胞核周围,同时磷酸化并一起进入细胞核(见图3左)。由于这种磷酸化同步开关,每天有成千上万的PER分子可以同时进入细胞核,维持稳定的昼夜节律。
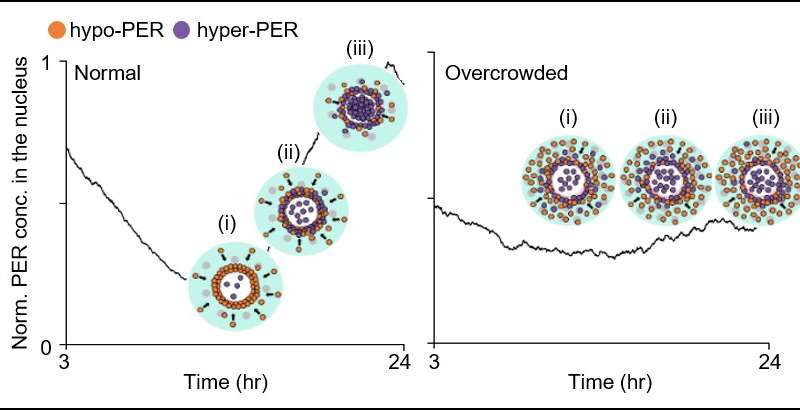
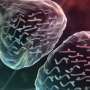
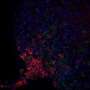
然而,当衰老和/或痴呆、肥胖等疾病导致细胞质充血时,蛋白质聚集物、脂肪空泡等细胞质障碍增加,阻碍了PER的及时凝聚分子(见右图3)。结果,磷酸化同步开关没有起作用,PER蛋白以不规则的时间进入细胞核,产生昼夜节律研究显示,睡眠-觉醒周期不稳定。
金教授说:“作为一名数学家,我很高兴能够帮助推进新的治疗策略,从而改善许多患有睡眠-觉醒周期不规律的患者的生活。”以这些发现为契机,我希望看到数学和生物科学之间更积极的思想交流和合作。”
进一步探索














用户评论