高胰岛素血症性低血糖的新疗法
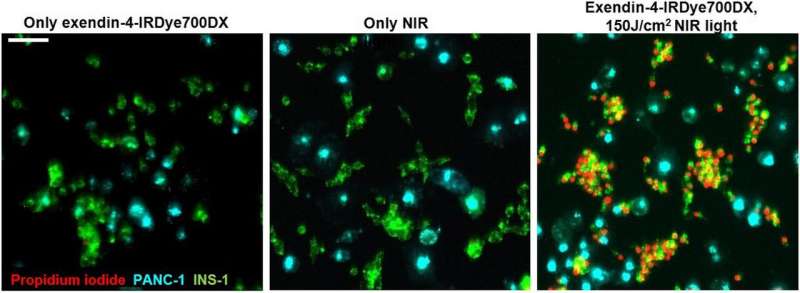
一种治疗高胰岛素血症性低血糖的新方法已被证明在靶向病灶上具有高度选择性,并且在减缓肿瘤生长方面有效,根据发表在11月号的研究核医学杂志。该新方法利用exendin-4- irdy700dx的受体靶向光动力治疗,诱导胰岛素产生细胞产生光毒性,导致高胰岛素血症性低血糖。
胰腺分泌胰岛素细胞通常是一个规范良好的过程;然而,不受控制的胰岛素过量生产可能会出现。在成人中,这种过度分泌通常是由胰岛素产生病变引起的,称为胰岛素瘤。在新生儿中,引起胰岛素过量的最常见原因是先天性高胰岛素血症。当过量的胰岛素产生导致危险的低血糖水平时,高胰岛素血症就发生了。长时间的高胰岛素性低血糖会导致癫痫,意识丧失,永久性脑损伤或脑死亡。
“高胰岛素性低血糖症的治疗具有挑战性,”martinboss说,他是荷兰奈梅亨内梅亨大学医学中心医学影像学系博士后研究员。目前的治疗包括侵入性手术而治疗低血糖发作的药物并不总是有效的,还会产生副作用。由于这些挑战,一种新颖的微创治疗成人和儿童高胰岛素血症性低血糖的选择是必要的。”
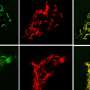
为了解决这个问题,人们建立了细胞和动物模型来承载胰高血糖素样肽1受体(GLP-1R)胰腺β细胞胰岛素瘤水平也很高。研究人员使用receptor-targeted光动力治疗将光敏分子irdy700dx与肽exendin-4(专门针对胰岛素产生细胞)偶联,照射GLP-1R细胞和异种移植物。在体外测量了受体靶向光动力治疗导致细胞死亡的疗效和特异性。示踪剂的生物分布,对细胞损伤的诱导及作用肿瘤的生长在体内进行测量以确定治疗效果。
以受体为靶点的光动力疗法被发现在GLP-1R阳性细胞中引起显著的特异性光毒性。在动物模型,示踪剂在GLP-1R阳性肿瘤中呈剂量依赖性积累。体内靶向受体的光动力疗法也能诱导肿瘤细胞毒性而不损伤周围组织,从而延长中位生存期。
Boss说:“这项技术为受体靶向光动力疗法的有效性提供了第一个证据,这种疗法已经被证明对几种癌症的胰岛素产生病变的治疗是成功的。”“在未来,这可能为高胰岛素性低血糖提供一种全新的、微创的、高度特异性的治疗方法,这将显著改善患者的临床管理。”













用户评论