胃癌致死性副作用的免疫蛋白IL-17A
胃癌是世界范围内导致癌症相关死亡的主要原因之一,以其在腹膜腔内传播的能力而闻名。除了引起其他器官的继发性肿瘤外,转移性胃癌细胞还会引发广泛的间质纤维化,或疤痕组织的形成,这可能比癌症本身更致命——肠梗阻、肾盂积水和黄疸都是胃癌相关纤维化的常见副作用。更重要的是,由于肿瘤内高压,密集的疤痕组织会干扰化疗药物到达其目标。
因此,预防纤维化可以改善预后胃癌病人。问题是,研究人员尚未发现纤维化的原因,更不用说如何预防了。
但在最近发表的一项研究中胃癌美国金泽大学(Kanazawa University)的研究人员发现肥大细胞在胃癌患者中,IL-17A触发腹膜细胞改变,导致间质纤维化。
该研究的主要作者、来自金泽大学癌症医学部的Katsuya Gunjigake解释了研究人员以IL-17A为目标的原因。
“IL-17A对免疫系统的过度刺激在风湿性关节炎和多发性硬化症等慢性炎症疾病中起着重要作用。它还与各种形式的癌症中肿瘤生长和扩散的增加有关。有趣的是,研究表明IL-17A会导致克罗恩病和肺部疾病在美国,没有人研究过癌症中组织纤维化和IL-17A之间的联系。”
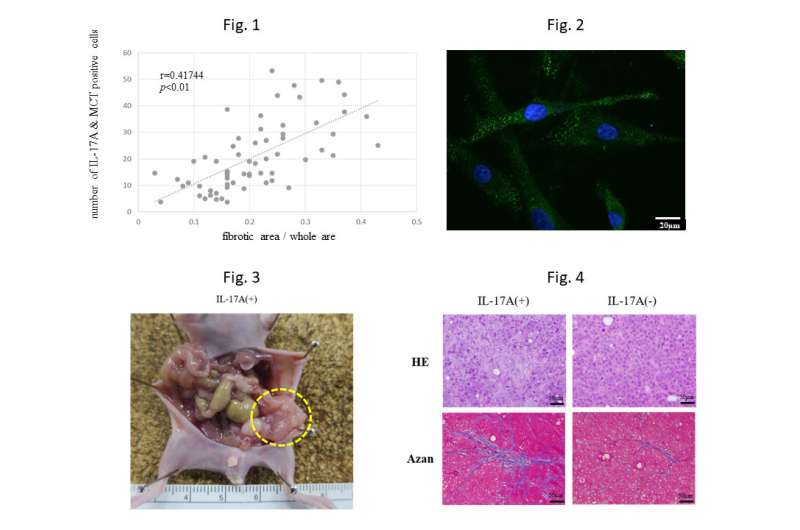
通过研究70名伴有腹膜播散的胃癌患者的癌组织,研究人员发现纤维化的程度由IL-17A的数量控制,IL-17A是由一组称为肥大细胞的白细胞产生的。
Gunjigake说:“肥大细胞通常与过敏反应有关,但也参与病原体防御和免疫耐受等。它们包含小颗粒这种颗粒充满了分子,如组胺、血清素和IL-17A,并在脱颗粒过程中被释放到细胞外环境。”
然后,研究人员给小鼠注射了人类腹膜细胞和胃癌细胞,并检测了IL-17A治疗的效果,得到了有趣的结果。
“IL-17A不仅增加了肿瘤的大小和纤维化的程度,它还改变了腹膜细胞的结构,增强了它们的侵袭和迁移能力,”负责的作者Sachio Fushida解释说。
“鉴于IL-17A在驱动纤维化中的明显作用,我们的结果表明,抑制肥大细胞脱颗粒可能是一种有前途的治疗策略,用于腹膜播散的胃癌患者。”
进一步探索











用户评论