2020年1月21日报告
生命与铁垂病的持续斗争
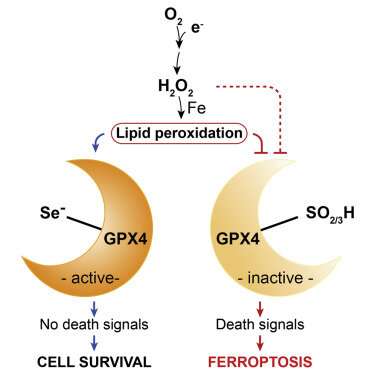
在自然过程中,多细胞生物经常需要消灭细胞。例如,在人类中,多余的尾巴、指蹼、错误思维产生的免疫细胞或结交不恰当的朋友的神经元可能都是健康的细胞,但它们需要一个干净的出口。另一方面,因突变或氧化损伤而受损的细胞对邻近细胞是一种直接威胁,在它们优雅地退出之前,往往需要更剧烈的刺激。
在每种情况下,编程细胞死亡或细胞凋亡,展开的独特变体。Ferroptosisis,一种特别令人讨厌的形式,在谷胱甘肽抗氧化系统的故障下提出,导致膜脂质过氧化的广泛自动启动。原因令人惊讶的是单数:酶GPX4的供应失败满足需求。虽然GPX4只是身体较大的八折谷胱甘肽过氧化物酶防御库中的一种特定工具,但它是唯一一个装备巡逻细胞及其细胞器的磷脂边界的工具。
最近的评论自然由Marcus Conrad和Derek Pratt提供了理解骨凋亡化学的坚实基础,以及我们如何将其弯曲到我们的优势。对于一件事,已经显示出多种肿瘤是唯一易受硬化的影响。适应化学疗法并面临转移的风险的癌细胞特别依赖于GPX4轴以存活。这使其成为药物有吸引力的潜在目标。
虽然铁在枯萎病途径中的含义是从展示铁螯合剂阻挡它的研究中的清晰,但是作者注意到,如何以及那里的不同形式的铁法尚未完全理解。一种线索是GPX4的特异性同种型在天然铁富含线粒体的内膜空间中丰富。在恶性裂解中,由于嵴破坏,线粒体缩小。该过程可以通过新的BBB可渗透的分子抑制Liproxstatin-1,如果被发现是安全的,可能最终会变成fda批准的医疗选择。
没有GPX4的生活很短。创造的帧突变突变过早截断GPX4蛋白完全消除其功能并导致称为Sedaghatian型脊柱型孢子瘤性发育不良(SSMD)的疾病。出生的婴儿具有这种极其罕见的病症通常不会超过30天内存活。raghav sanath出生在一年半前,被发现有ssmd。他的特定变体是GPX4的外显子6中的常血型隐性纯合突变C.647g> a。它位于19P13.3(19-1106433)的染色体上,并且对于遗传性白话来说,它可以找到附加号码(NM_001039848.2)。
该CGC> CAC取代在蛋白质中的效果是在蛋白质中一个位置的正常精氨酸(R)的组氨酸(H)中换流。在GPX4的较短形式上,该位置被编号为R152H,而在较长的形式上,它是R179H。在一些列表中,包括可切割的靶向序列,在这种情况下,它因此将作为R216h提供。虽然这种看似保守的替代一个基本氨基酸的效果可能不被认为是一种激进的突变,但其在GPX4中的效果是未知的,这是迫切需要生物物理学建模的东西。在其他蛋白质中,H-FOR-R替换赋予pH敏感性增加甚至与癌变有关。
Raghav的父亲Sanath Ramesh是一位全职高级软件工程师,现在已经使他的企业成为SSMD的治疗方法。他组建了一支专家团队,包括西雅图儿童医院和圣地亚哥的乌克西儿童克里斯汀·瓦比的医生罗布斯Saneto,尽快探索治疗。他的直接目标是筹集300万美元来执行药物开发管道他仔细制定了。这将涉及重新估算批准的药物,入围额外的新型硬化调节剂,并分析诊断生物标志物疾病进展和治疗。Sanath的所有这些努力都是经线驱动的推动,了解GPX4的疾病生物学。

这是我们可以做到的,在某种程度上,已经做到了。它以一个简单的问题开始:为什么GPX4如此重要?如我们所见,GPX4将一种特殊的解毒能力带到一个特殊的地方(细胞膜),主要是一个特殊的细胞器(线粒体)。但这种独特的排毒能力是什么呢?简而言之,答案是硒——更具体地说,GPX4 mRNA中的氨基酸半胱氨酸的共翻译编码成硒半胱氨酸(Sec),这是通过劫持UGA停止密码子在整个物种进化过程中得以实现的。虽然目前已知至少有25种人类蛋白质使用硒,但只有GPX4被发现提供一个明确定义的基本需求。
这种基本要求在所有较高的生命形式所采用的遗传密码的整个进化过程中留下了刺。它可以概括如下:生命死亡的生存密切依赖于大脑的精英速度冠军的能力 - 即普遍存在,迅速烧制,帕瓦仑霉素阳性胃肠杆菌 - 解毒 - 解毒了他们的自由基损伤膜在高活动期间待持。未通过这种安全机制,这些神经元的惯例活性可预测螺旋致致命的癫痫发作。
马库斯·康拉德和其他人在过去几年里对Sec的研究中费尽心思拼凑出的结论是,虽然硫可以让你进门,但只有硒可以让你出来。换句话说,当实验控制小鼠在GPX4的活性位点上保留良好的硫基半胱氨酸而不是Sec时,它们确实保留了生全面发展,但会在几周后死亡,因为它们盛开的中间神经元很快就会被致命的铁垂病摧毁。这一过程可以比作喷气发动机在热力和机械极限附近工作。如果被推入陡坡,飞机可能会在一段时间内继续提供全部动力,但由于空速大幅降低的额外限制,它无法再摆脱自身的热量。
为什么selenium?
在全球范围内思考一下,硒比硫在含量不那么丰富,其分布和生物利用度非常差异。虽然梦想家可能会推测其他行星上的潜在生活是否会使用与我们相同的遗传密码,但我认为真正的问题是硒的分布虚构的世界,以及它的生物是重新潮成的。它需要大约25摩尔ATP,以将1摩尔半胱氨酸插入生长蛋白质中。根据特定物种,大多数不同的GPX同种型在其活跃部位进行半胱氨酸。将Selenium添加到混合中需要大量的费用,更不用说遗传密码自身重新引发的巨大存在风险。为什么有人想这样做?
硒比硫显着大。它也更加可极化,其外部价电子更松散地保持。结果,它是更好的亲核官员会与之反应反应性氧气比硫快,但它缺乏π-粘结的特征意味着它也可以更容易地减少。这些性质的组合意味着在自然中用硒代替硫含量,导致抵抗永久氧化的含硒的生物分子。
与硫相比,硒蛋白的另一个考虑因素是其较低的氧化还原电位。GPX4-Cys变体在其底物浓度超过时经历过氧化和不可逆失活。另一种哺乳动物硒蛋白TXNRD2也表现出这种过度氧化行为,这表明硒酸盐相对于硫酸盐的关键优势可能存在于抗过度氧化。
在康拉德的论文中找到的许多人寿课包括许多传统氧化过程的现实现实,不再切割它。例如,像“脂质过氧化”和甚至“ROS'一样的术语通常是高度暧昧的。过氧化意味着脂质的二氧化或脂质氢过氧化物的形成。但是,在其常见的使用中,该术语在哪个术语不提供产品是否形成的差异通过自动氧化或通过酶催化方法自发的方式。
酶脂质过氧化主要由脂氧基酶,非血红素二氧化碳酶和较小程度的环氧氢酶进行。随着上述作者所知,推测GPX4中的SER的存在令人遗憾的是保留保留,以适应可以用于细胞信号传导目的的细胞过氧化物而不影响细胞活力。与高反应性分子一样,如例如超氧化物,通常会模糊代谢潜在病理上毒性副产物的差异和基本调节信号分子的差异。
基因组宽的逆向遗传筛鉴定了激活硬质裂菌所需的另外两种基因。它们是酰基-CoA合成酶(ACSL4)和磷脂酰胆碱酰基转移酶-3(LPCAT3)。另外的研究表明,凋亡诱导因子线粒体-2(AIFM2)的过表达,一种能够从泛醇再循环泛醇的氧化还原酶可以完全补充GPX4损失。AIFM2已被重新命名为脱裂抑制蛋白-1(FSP1)。根据Sanath的说法,FSP1似乎是一个有吸引力的目标,但目前,没有可行的方式在人类中安全地过表达它。
萨纳斯组织了一次将于今年4月举行的会议,以便聚集在一起临床和研究努力一起住在同一个屋檐下。嘉宾演讲人将包括铁瘫的发现者Brett Stockwell和药物发现和N-of-1研究的真正先驱Ethan Perlstein。这个令人兴奋的新领域的最新发展可以在社交媒体#CureGPX4上追踪到。
进一步探索
©2020 S欧宝app网彩cience X Network













用户评论