帮助胰腺癌细胞避免饥饿的机制
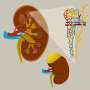
一项新的研究揭示了一种机制,它通过劫持一个从周围环境吸收营养的过程,帮助胰腺癌细胞在致密肿瘤中避免饥饿。
由纽约大学格罗斯曼医学院的研究人员领导的这项研究解释了ras基因的变化是如何促进90%的胰腺癌患者的异常生长的,同时也加速了提供生长所需的构建模块的过程。
这个过程被称为大胞饮作用,它吞噬蛋白质和脂肪,这些蛋白质和脂肪可以被分解成氨基酸和代谢物,用于构建新的蛋白质、DNA链和细胞膜。癌症细胞该研究的作者说,手头没有这些资源就无法繁殖。
该杂志于12月11日在线发表自然,新的工作确定了关键的分子步骤的编组癌症细胞提高微胞饮现象。
“我们发现了一种与营养供应相关的机制,我们相信可以用来阻止RAS突变肿瘤第一项研究的作者克雷格·拉米雷斯博士说,他是纽约大学医学院生物化学和分子药理学系的博士后。
剧院的操作
具体来说,研究小组发现RAS突变进一步激活蛋白质SLC4A7,它能使一种叫做碳酸氢盐依赖性可溶性腺苷酸环化酶的蛋白质激活蛋白激酶a。这反过来又被发现改变了一种叫做v- atp酶的蛋白质的位置。
研究人员说,通过将v- atp酶作用的区域从细胞深处转移到细胞外膜附近,该反应可以将RAC1所需的胆固醇转移到细胞膜上。v- atp酶在外膜附近的聚集,以及Rac1的相关定位,使细胞膜在大胞吞过程中暂时膨胀,翻转,形成营养吞噬袋(囊泡)。
在细胞培养研究中,用SLC4家族抑制剂S0859处理突变RAS细胞可显著降低RAS依赖的v- atp酶在外膜的定位,以及对微胞增多症的抑制作用。
此外,对人胰导管腺癌(PDAC)组织的分子数据分析显示,SLC4A7基因在肿瘤中的表达比在正常胰腺组织中的表达高4倍。
该研究小组还表明,沉默胰腺癌细胞中的SLC4A7基因可以减缓或缩小小鼠的肿瘤。14天后,与活性基因相比,含有SLC4A7基因的小鼠肿瘤中62%的肿瘤生长速度减慢,31%的肿瘤出现萎缩。
“我们现在正在寻找可能抑制SLC4A7或v- atp酶作用的候选药物,作为潜在的未来治疗方法,以阻止大细胞增多症,”该研究的资深作者达夫娜·巴-萨吉博士说。高级副总裁他是科学副院长,也是纽约大学朗格尼健康中心的首席科学官。“这两种蛋白质原则上都是很好的靶标,因为它们与癌症生长有关,并在肿瘤附近工作癌症细胞表面,通过血液输送的药物可以到达细胞表面。”
进一步探索