血细胞可以持有主时钟背后老化

血液细胞衰老的关键,根据新的研究凯斯西储大学医学院的。在发表的一项研究衰老细胞研究人员发现,人类血液细胞有一个内在的时钟保持稳定甚至在移植。研究人员说时钟可以控制人类衰老和可能构成血液癌症。
沼泽松山,兽医学博士博士,细胞生物学家和医学副教授凯斯西储大学医学院的领导的一个国际研究小组的研究人员研究了时钟。团队测量血液细胞移植细胞年龄从健康的捐赠者白血病患者,关注捐助者与接受者对截然不同的年龄。
“这项研究是有关青春之泉,“松山说。“我们发现年轻的血液细胞在老年人保持年轻。没有加速老化的年轻老人体血液细胞。”Matsuyama's team found the other direction was also true—blood cells from adult donors transferred to a child stay older. The cells retained their intrinsic age nearly two decades after transplant.
他们的固有稳定性表明血细胞的主时钟人类的衰老,因为它们不容易受到环境的影响,松山说。
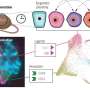
研究显示血细胞DNA methylation-chemical基团DNA保留表观遗传模式可以用来计算自己的年龄。尽管在供体和受体之间巨大的年龄差距(49岁),移植血液的DNA甲基化年龄反映了供体的年龄,即使经过多年的接触对方的身体,作者写道。松山说,“DNA功能作为我们时代的计时员。”
DNA甲基化是一个年龄的预测第一次描述了松山的合作者在2013年的研究中,生物统计学家史蒂夫•霍博士,加州大学的洛杉矶。“他发现公式。机制,细胞在体内是否同步DNA甲基化时代,松山解释不清楚。”“我不是数学家。我是一个细胞生物学家。所以,我们合作研究表观遗传机制的时钟在实验系统在我的实验室。”
松山测试血液样本定期收集作为移植的一部分监控、的帮助情况综合癌症中心。他扩大了样本库通过白血病奥斯陆大学的研究人员,在挪威,听说他在2016年的工作梯形专题讨论会衰老在圣达菲举行,新墨西哥。霍法分析细胞年龄使用353种不同甲基化网站上发现血细胞DNA。
在一起,研究人员首次提供了实验证据,血液细胞的衰老是细胞内在,而不是规定与其他细胞类型的交互。
他们现在努力识别机制,可以改变时钟。“癌细胞的钟坏了,“松山说。在癌细胞DNA甲基化模式是不稳定的血细胞和经常显示奇怪的老化- 200或5岁50岁的病人,例如。“这与实际年龄不匹配。”Matsuyama cautions that this is why, although it may sound appealing, he doesn't yet recommend "therapeutic" cell infusions to try to maintain one's youth.
“我们不知道血细胞作为一个主时钟同步其他细胞。我们只是还不知道,”他说。
相反,松山的团队正在努力理解为什么后生年龄差异存在于肿瘤细胞,以及它们如何能被克服。“可能是通过打开或关闭特定基因在细胞内,我们就可以重置时钟。”
最近的研究表明人类的DNA年龄细胞可以用作生物标志物预测与年龄有关的疾病的风险,这样的吗阿尔茨海默病,心血管疾病,其他人。去年,霍和松山帮助发布一个文章报道称,DNA年龄显著加速早衰症患者患有早衰。松山和他的同事们现在有几项研究正在揭示年龄相关性DNA甲基化的机制,并理解因素如饮食,锻炼,和氧含量影响表观遗传的时钟。
更多信息:阿恩Søraas et al,表观遗传的年龄是一个细胞内在属性在人类造血细胞移植,衰老细胞(2019)。DOI: 10.1111 / acel.12897