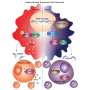
PIM-2蛋白激酶调节t细胞活动不同于PIM-1或PIM-3同种型

PIM-2蛋白激酶负面在移植和肿瘤免疫调节T细胞反应,尽管PIM-1和PIM-3积极的监管机构,南卡罗来纳医科大学的报告(音乐)调查人员在5月21日在线发表的一篇文章中,2018年《临床研究杂志》(青)。阻塞PIM-2在同种异体骨髓移植(BMT)大大加速移植物抗宿主病(GVHD)。与自体T细胞过继免疫治疗,沉默PIM-2在T细胞产生强劲的肿瘤免疫,突出PIM-specific抑制的重要性。
PIM的蛋白激酶家族包含三个亚型,PIM-1, PIM-2 PIM-3,非常相似的结构。因为他们会影响细胞的存活和增殖能力,该集团在癌症被认为是一种很有前途的治疗目标。此外,pan-PIM抑制(阻塞所有三个亚型)通常用于癌症治疗。
因为亚型是如此相似,他们函数的假设是,类似的方法。文章中,然而,在美国音乐的一个研究小组由Xue-Zhong Yu,医学博士系的教授微生物学和免疫学和SmartState赋予椅子在癌症干细胞生物学和治疗目的就是癌症中心,表明PIM-2激酶调节T细胞具有独特的活动,反对PIM-1 PIM-3。
“这激酶家族在癌症生物学研究相当广泛。我们知道肿瘤激活或将在这些激酶生存更好,因为这三个亚型帮助保护癌症细胞从死亡使它们对化疗产生抗药性。这就是为什么不少公司已经开发出pan-PIM抑制剂对癌症治疗,”Yu说。
虽然大多数研究都集中在癌症生物学的PIM激酶的作用,对他们如何影响主要T细胞和免疫应答。于和他的团队开始试图了解这些激酶调节T细胞反应BMT和实体肿瘤。
同种异体BMT是一个重要的治疗白血病等血液癌症,因为,即使化疗和放疗,少量的肿瘤细胞可以留在血液中,使恶性肿瘤复发。取代病人的骨髓是最好的方法来防止这一点,但是一个理想,生理上匹配的捐献者通常不是可用的。不相配的捐赠者,移植物抗宿主病的风险越高,供者细胞触发免疫反应攻击患者的正常组织,导致高发病率和死亡率。研究人员一直在寻找方法来提高BMT成功通过减少GVHD发生率,同时保留供者细胞的抗肿瘤反应。
余的团队开始通过测试的假设与雷帕霉素抑制PIM激酶将协同工作,免疫抑制剂药物,控制移植物抗宿主病的发展。使用临床前小鼠模型,观察击出每一个PIM同种型,分别在各种组合,移植物抗宿主病诱导的影响。
“我们认为,如果这些激酶并行工作,然后阻塞所有三个途径同时会提高治疗效率,”Yu解释道。“但是当我们测试每一个,我们看到PIM-2真的站从他人和主导作用。我们发现,T细胞缺乏PIM-2已经极大地提高了激活和致病性导致移植物抗宿主病。”
相比之下,阻塞PIM-2创建高度激活,激进的T细胞攻击癌症。“我们的研究结果BMT模型非常健壮。当我们移植的正常T细胞数(缺乏PIM-2),老鼠患上严重的移植物抗宿主病和死亡超级速度10天。我们必须保持降低T细胞的剂量,”Yu说。团队甚至最终发现的只有50000 PIM-2缺乏T细胞导致移植物抗宿主病,而这个数字的野生型,控制T细胞诱导移植物抗宿主病的能力。
这些结果表明,PIM-2激酶扮演着主导的角色在调节T细胞在诱导致病性PIM-2 GVHD和揭示先前定义的角色:强有力地抑制T细胞alloresponses和GVHD感应。结果显示,虽然PIM-2负调节T细胞,PIM-1和PIM-3积极调节T细胞活化。
“想象疗法是一辆车,”Yu解释道。“如果你想要它更快,你可以踩油门通过提高积极分子调节T细胞,或者你可以移除负面的刹车通过阻断分子调节T细胞。阻塞PIM-2就像删除从一辆汽车刹车然后有更多的力量消灭恶性肿瘤,尽管代价GVHD的副作用。”
接下来,小组调查PIM-2封锁在一个坚实的,同系的肿瘤模型,缺乏PIM-2癌细胞移植到老鼠。玉惊讶的结果。“当我们注射肿瘤细胞系,肿瘤不能生长在PIM-2阻止老鼠,”Yu说。“控制小鼠肿瘤迅速增长,但没有PIM-2分子可以完全拒绝的小鼠肿瘤。这是一个大惊喜。分子很少如此强大。”
这一发现强调了潜在PIM-2封锁的癌症免疫疗法。
这是第一次的独特活动PIM-2激酶在T细胞区别于其家庭成员,PIM-1 PIM-3。这些发现提高pan-PIM抑制的担忧,这可能缺点当预期的效果是抑制免疫反应和T细胞无力。此外,可能并不适用于同种异体BMT PIM-2封锁,因为它可能会加剧移植物抗宿主病,而PIM-1和PIM-3封锁可能减轻GVHD。
“这项研究强调了需要特定抑制剂和行使谨慎使用pan-PIM抑制剂,”Yu解释道。“同一家族激酶可以扮演不同的角色,所以我们必须更加谨慎和理解上下文的亚型我们想阻止,因为他们可能不会以协同的方式工作。当我们做科学研究的教训是,我们必须保持一个开放的心态。这激酶家庭一直得到广泛的研究,但我们看到完全出乎意料的结果,当我们研究它们在不同细胞和不同的系统。”
更多信息:阿奴萨拉Daenthanasanmak et al, PIM-2蛋白激酶负面在移植和肿瘤免疫调节T细胞反应,临床研究杂志(2018)。DOI: 10.1172 / JCI95407