内存分子通过校准钙来限制可塑性
大脑有着令人难以置信的能力来支持一生的学习和记忆。每一次新的体验都会从根本上改变大脑中称为突触的细胞之间的连接。为了适应突触的改变,大脑的某些区域具有高度的可塑性,这意味着有能力适应传入的信息。海马体是大脑记忆的重要结构,它是整个大脑中可塑性最强的细胞之一,利用突触可塑性的过程来保持准备和灵活。
坐落在高度之间塑料ca1和ca3区,相当不灵活神经元区域CA2不容易进行突触可塑性,对其近邻的功能性鲜明对比。一旦被低估,CA2地区现在被理解为内存的社会,空间和时间方面以及咖啡因的认知促进效果的目标是重要的。确定赋予可塑性独特电阻率的独特因素可以为学习和记忆的神经基础提供重要的洞察。
为了解开可塑性的谜团,马克斯·普朗克佛罗里达神经科学研究所(MPFI)的研究人员与埃默里大学和国家环境健康科学研究所的研究人员合作,首次发现了ca2富集蛋白RGS14的新作用,并为其限制可塑性的机制提供了见解。Ryohei Yasuda实验室博士后研究员Paul Evans博士及其合作者于2018年5月在该杂志上发表了一项研究eNeuro链接RGS14的抑制可塑性的能力钙监管。RGS14是一种特殊的支架蛋白,包含一种独特结构域的混合物。之前Evans和他的同事在蛋白质组学研究中探索了这些域,建立了两个新的RGS14相互作用伙伴:CaMKII,钙信号蛋白和钙调蛋白钙结合蛋白和关键的钙调节剂。为了引发Ca1神经元中的突触塑性的信号级联,需要钙进入细胞中的膨胀来推动Camkii和钙调蛋白的活性。由于这种关系,RGS14准备用作钙调制器,在CA2中浇注可塑性。
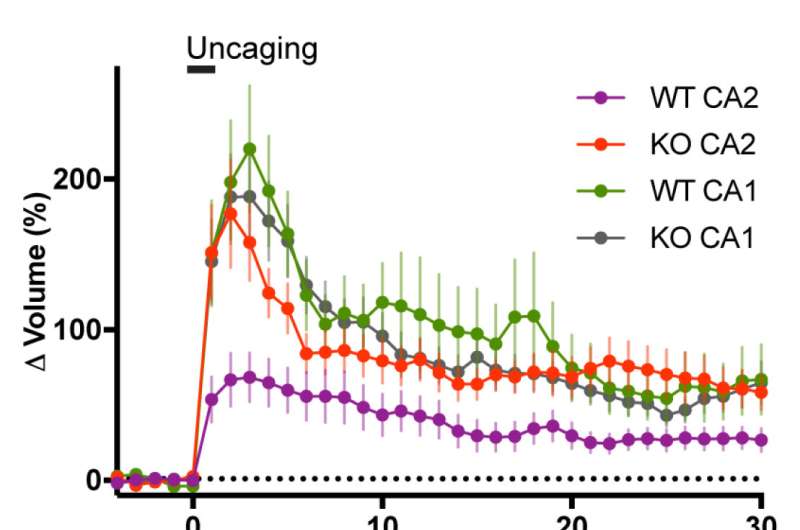
为了验证这种建议的关系,越来越详细探测evans和合作者,称为长期增强(LTP)的掩蔽形式,当移除RGS14时,在CA2神经元中唤醒。值得注意的是,除了强大的CA2之外,缺少RGS14的小鼠还显示增强学习突触可塑性,与CA1报告的水平相同。为了确定这种潜在的CA2可塑性是否与CA1的钙驱动机制类似,该团队使用了精确的药理抑制剂,针对缺乏RGS14的小鼠的关键钙信号分子。引人注目的是,这些抑制剂在CA2缺乏RGS14的神经元中消除了新发现的LTP,表明CA2中钙信号的必要性,并揭示了与CA1可塑性机制的相似性。
Evans接下来的研究证实了钙信号是CA2静态可塑性的重要组成部分钙流入在LTP中的小神经元隔室中称为树突脊柱,来自含小鼠并缺乏RGS14的CA2神经元。含有RGS14的小鼠的血管中的钙瞬变明显小于缺乏RGS14的小鼠的血小鼠,表明RGS14在调节CA2神经元中的钙水平方面发挥着重要作用。此外,在Ca1区表达时,RGS14在缺乏蛋白质的Ca2神经元中的RGS14缺乏塑性度并显着降低可塑性。增加的细胞外钙水平逆转了塑性的取消,加强了RGS14通过调节钙的可塑性限制特性的观点。

“RGS14似乎是特殊的,作为将制动器的塑料放在存在的分子因素,使专门的内存编码能够进行专门的记忆编码。建立更加了解促进脑区之间细微差异的分子化妆,如在CA1和CA1中所见的微妙差异CA2,将使我们更好地了解利益学习和记忆的机制,“埃文斯博士。
进一步探索










用户评论