左起:Amjad Javed博士和陈海燕。图片来源:阿拉巴马大学伯明翰分校
Amjad Javed博士和阿拉巴马大学伯明翰分校的同事们发现了转录因子特异性蛋白7 (Sp7)在牙齿发育中的关键作用。
UAB大学的研究人员利用动物模型发现,缺乏Sp7会阻碍两种帮助形成牙齿的特化细胞的成熟。这样的基本知识发展对牙齿和骨骼的研究增加了对颅面畸形的理解,这是人类最常见的出生缺陷之一。
转录因子是与DNA相互作用来开启或关闭基因的蛋白质。在胚胎中,它们引导从单个受精卵分化为形成身体不同组织和结构的所有细胞。其中一个复杂的结构就是牙齿。
哺乳动物的牙齿在胚胎发育时就开始发育,尽管它们只在出生后才长出来。发表在《骨骼和矿物研究杂志他使用了一个Sp7基因的两个副本都发生突变的老鼠模型。
以前人们知道Sp7是骨骼发育所必需的。Sp7双突变的胚胎完全缺乏矿化骨。在人类中,Sp7基因的突变会导致成骨不全,这种情况会影响骨骼和颅面结构的发育。然而,Sp7在胚胎牙齿发育中的作用尚不清楚。
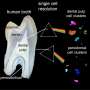
通过对缺乏Sp7的小鼠的研究,Javed和他的同事们发现,即使这些动物缺乏矿化的牙槽,它们的牙齿初始形态形成是正常的。然而,牙齿的发育并没有继续——动物们不能产生正常的牙本质(构成牙齿大部分的硬组织),也不能产生正常的牙釉质(覆盖牙齿的超硬基质层)。这是由于成牙细胞和成釉细胞的增殖、成熟和极化减少。
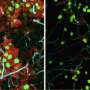
成牙本质细胞在发育中的牙齿内并排排列,形成一层沉积牙本质的柱状细胞。同样,成釉细胞在发育中的牙齿外面并排排成一排,形成珐琅质。
没有Sp7,这些动物的牙齿小而畸形,成牙本质细胞和成釉细胞没有在成牙本质细胞前和成釉细胞前阶段成熟,这是通过缺乏成熟细胞标记来衡量的。成牙本质细胞和成釉细胞数量较少,排列紊乱。
研究人员发现,正常小鼠的Sp7只在产生成牙本质细胞的牙间充质组织中表达;它在产生成釉细胞的口腔上皮中不表达。由于已知成纤维细胞生长因子(Fgf)家族的13个不同成员在小鼠牙齿发育过程中作为两种不同组织(牙间充质和口腔上皮)之间的信号蛋白,Javed和同事们在缺乏Sp7的小鼠中寻找Fgf配体的变化。
他们发现Fgf3和Fgf8配体在正常情况下是丰富的牙齿发育,缺失Sp7的动物的切牙和臼齿明显缺失。提示成釉细胞成熟失败的原因是间充质与上皮间交叉信号通路的中断。此外,他们发现Sp7转录因子直接控制Fgf配体的基因表达。
总之,UAB的研究人员得出结论,Sp7在成釉细胞和成牙本质细胞的分化中是必须的,但在初始阶段不是牙形态发生。
更多信息:裴智明等人。成釉细胞和成牙本质细胞增殖和分化所需特异性蛋白7骨骼和矿物研究杂志(2018)。DOI: 10.1002 / jbmr.3401
期刊信息:骨骼和矿物研究杂志
所提供的阿拉巴马大学伯明翰分校