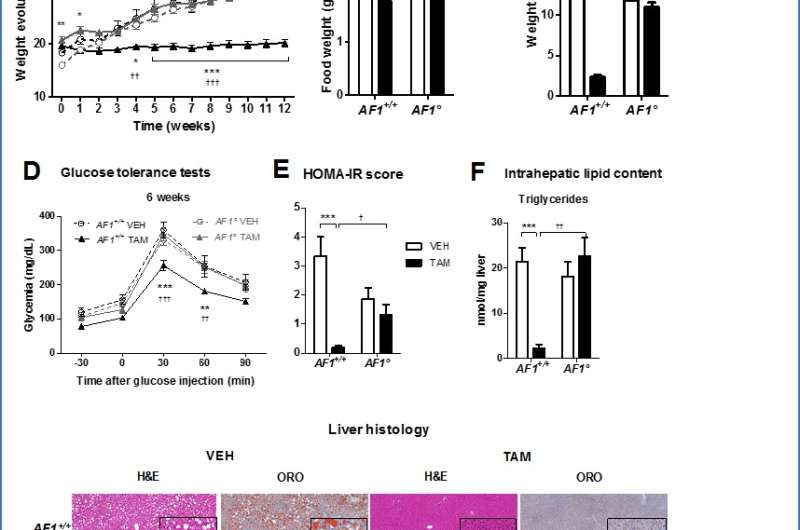
每周记录体重进化(A)和食物摄入(B)。C:在HFD的12周后,通过磁共振成像(Echomri)评估身体组成(脂肪质量)。D:I.P.在HFD的6周后进行葡萄糖耐量试验。E:胰岛素抵抗胰岛素抵抗估算胰岛素抵抗(HOMA-IR)评分估算,在HFD 12周后计算。F:在牺牲中评估肝内中性脂质含量和肝脏组织学。肝脏切片上苏木精和曙红(H&E)和油红O(ORO)染色的代表性图像。插入显示更高的放大率。数据表示为平均值±SEM。* P <0.05,** P <0.01,*** P <0.001。 Scale bars: 100 mm (Liver Histology); 50 μm (G, insets). Original magnification, ×40 (insets). VEH-Vehicle alone; TAM-Tamoxifen treated. Credit: The美国病理学杂志
Tamoxifen是一种选择性雌激素受体调节剂,是雌激素受体阳性乳腺癌内分泌治疗的金标准。他已知他莫昔芬具有代谢效应。新的研究美国病理学杂志报道称,该药物还可以防止肥胖,脂肪肝脏和患有高脂饮食的女性小鼠中的胰岛素抵抗力,卵巢被删除。该研究还能够确定哪些雌激素受体在这些保护作用下进行,从而开放新疗法以治疗这些条件的可能性。
“过去二十年来,雌激素受体α(ERα)已被鉴定为能量和葡萄糖稳态的关键调节因子,并因此提出了开发与肥胖相关的代谢障碍的新的治疗策略,例如2型的有希望的目标。糖尿病和非酒精性脂肪肝病。然而,了解ERα激活赋予的代谢保护机制是一个至关重要的挑战,“Pierre Gourdy,MD,博士,Inserm UMR1048,Institut desMaladiesmétaboliqueset cardiovularies(法国)(法国))。
除去卵巢的小鼠喂养高脂肪饮食并用两种治疗治疗Tamoxifen或者安慰剂12周。调查人员发现他莫昔芬预防重量增长,其与对照相比的食物摄入量显着降低。他莫昔芬治疗老鼠不太可能发展葡萄糖不耐受,胰岛素抵抗,以及肝脏中脂肪的沉积物。
研究人员知道ERα通过称为ERα-AF1和ERα-AF2称为ERα-AF1和ERα-AF2的两种激活功能来施加其效果。Tamoxifen根据其组织/器官靶标作为ERα-AF1激动剂或ERα-AF2拮抗剂。为了更好地了解他莫昔芬代谢效应的潜在的分子机制,科学家对遗传造成的小鼠遗传地造成的,用于整个ER-α(ERα - / - )或仅具有Tamoxifen或安慰剂的ERα-AF1(AF1-/ - °)并将结果与野生型小鼠(ERα+ / +或AF1 + / +)进行比较,接受了类似的治疗。所有的小鼠都喂养高脂肪饮食。
预防高脂饮食- 诱导葡萄糖不耐受那胰岛素抵抗和Erα-AF1缺乏的小鼠中,Tamoxifen滥用脂肪肝(脂肪变性)和脂肪肝(脂肪变性)。根据Gourdy博士,“总的来说,这些数据表明,通过Tamoxifen激活ERα-AF1足以引起体内的代谢保护作用。”此外,研究人员发现,通过Tamoxifen选择性激活ERα-AF1也调节了最肝脏代谢基因。
“完全是,本研究首先表明了代谢效应根据他们的更年期状态,他莫昔芬以及ERα的其他选择性调节剂,应该在女性中谨慎重新考虑。它还开启了对令人肥胖相关并发症的治疗令人肥胖的药物战略,以引起选择性ERα-AF1激活的药物策略,“Gourdy博士。
更多信息:“雌激素受体α活化功能-1的选择性激活足以防止小鼠的肥胖,脂肪变性和胰岛素抵抗力”。美国病理学杂志(2017)。DOI:10.1016 / J.AJPath.2017.02.013
信息信息:美国病理学杂志
由...提供elewsvier.