2015年11月18日报告
溶血性尿毒症综合症:寻找最佳治疗方案与世界上最广泛的药物之一
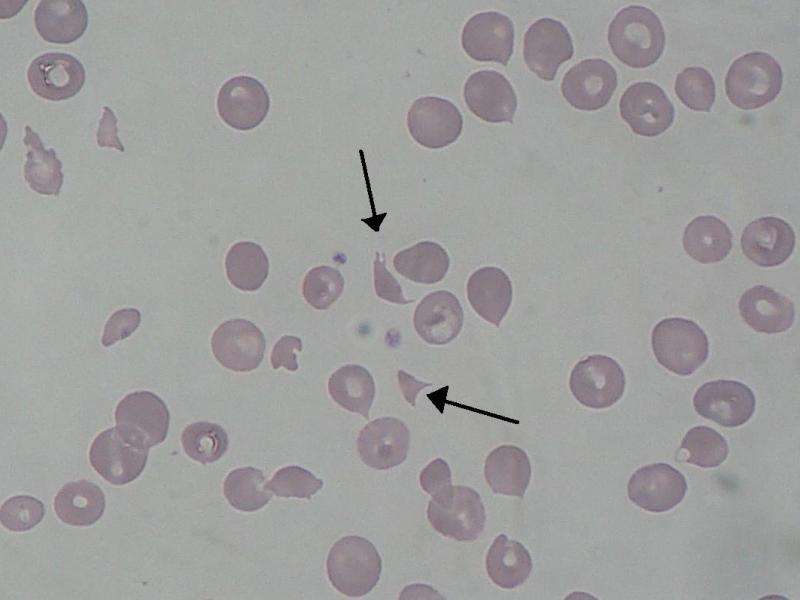
溶欧宝娱乐地址血性尿毒症综合征(HUS)是一种严重的疾病,可导致肾功能完全丧失。大多数溶血性尿毒病例是由感染产生志贺毒素引起的大肠杆菌德国2011年流行病中众所周知,导致845名所记录的HUS病例和54人死亡(1)。
一种罕见的,但更严重的典型形式的溶血性尿毒综合征(摘要)不是由感染引起的,但是是自发产生的超过50%的情况下结束阶段肾脏疾病进展(2)。这种形式的疾病是由于身体的攻击自己的补体系统在毛细管内壁(内皮细胞)肾脏的肾小球。
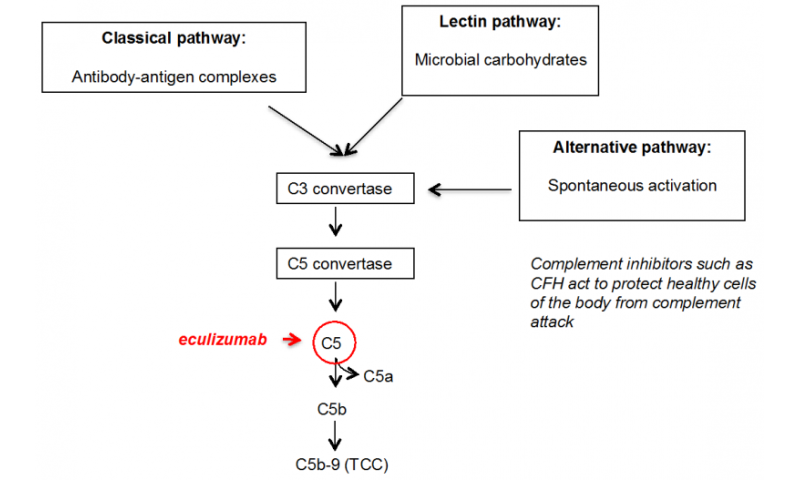
补体系统是先天免疫系统的一部分,由在血液中循环或与细胞结合的蛋白质组成。补体无活性时,其成分以无活性前体的形式存在。当补体被激活时,前体通过蛋白水解反应被修饰。补体激活的主要目的是消除病原体。补体可以通过三种途径被激活:经典途径、凝集素途径和替代途径(图1)。虽然经典途径和凝集素途径的激活需要触发器,如抗体抗原复合物或来自细菌表面的碳水化合物的存在,但替代途径可以自发地被激活。身体的健康细胞受到补体抑制剂的保护,免受补体的攻击。
目前,替代补体途径缺陷在约60%的Ahus患者中鉴定(2,3)。这些是编码替代补体途径蛋白的基因中的突变,或损害重要补体调节因子H(CFH)功能的自身抗体。
直到最近,aHUS患者的治疗一直是一项极具挑战性的任务(3)。血浆治疗是指患者接受健康个体的血浆,引入功能正常的补体成分。在一些患者中,这种方法有助于保存肾功能,但它在别人身上不足。在Ahus介导的肾功能衰竭的情况下,疾病的性质也存在严重的并发症。大多数在Ahus受影响的补体蛋白质在肝脏中产生。因此,在肾功能衰竭和移植的情况下,移植物中的Ahus复发存在高风险(高达100%)。这种问题的一种方法是进行双肾肝移植,这对患者来说是非常危险的。
2011年,补体抑制剂eculizumab(商品名Soliris)被批准用于治疗aHUS患者,标志着该疾病的治疗进入了一个新时代。
Eculizumab是一种针对补体成分C5的人源化单克隆抗体(图1)。在补体激活过程中,C5分裂为C5a和C5b。过敏素片段C5a增强血管通透性并通过趋化介导白细胞迁移。另一方面,C5b与补体蛋白C6、C7、C8、C9共同形成末端补体复合体(terminal complement complex, TCC),通常会导致致病菌裂解,如Neisseria Meningitidis.并且在没有有效的补体控制的情况下,也可以粘合健康的细胞。生态蛋白可与C5结合并防止其活化进入C5a和C5b,从而在该阶段阻断互补激活。
虽然Eculizumab对Ahus进行了非常有前途的处理,但它非常昂贵。成年患者每年约400,000欧元(427,000美元),对医疗保健系统造成巨大压力。目前的食品和药物管理局(FDA)和欧洲药物局(EMA)指导方针建议每两周用生态治疗终身治疗(最小婴儿三周),以防止AHU复发。本建议书在临床实践中受到质疑,主要是由于以下担忧:脑膜炎球菌感染和败血症的风险增加,可能导致可能导致生态的抗体的中和抗体,以及这种处理的极高成本。
已经尝试停止对康复患者的治疗(4)。在一些病例中,这导致了新的aHUS发作;在另一些情况下,却没有。有人认为,补体系统中存在某些突变(如CFH突变)的患者停药后aHUS复发的风险更大,但还需要进行更多的研究来验证这一假设。
虽然完全停止治疗的安全性仍然是一个开放的问题,但基于患者个体需求的治疗优化显然是重要的。目前的给药方案仅针对体重< 40kg的儿科患者进行体重调整。所有其他患者接受相同的剂量;因此,一个体重为50公斤的病人和一个体重为150公斤的病人将按照相同的方案进行治疗。
个体化方法的缺乏,部分原因是缺乏快速和可靠的检测来监测患者eculizumab的补体抑制能力。这些试验应提供可靠的数据,以确定在所选择的治疗方案(更低剂量或更长的输注间隔)下,补体是否仍被完全阻断。
最近,已经公布了几种体外方法,用于评估生态蛋白封锁(5,6)。所有这些方法都基于以下事实:通过使用特异性抗体,微生物组分或培养的细胞,可以在体外在血清样品中触发补体激活。补体激活导致可测量的补体激活产品,例如TCC。在完整的生态灭绝阻断的情况下,未观察到激活时TCC水平的增加。最近的一项研究提出了优雅的方法来估计Eculizumab是否给予访问(7)的患者。在该方法中,在活化之前用对照人血清稀释患者样品。结果表明,在目前的剂量方案下,在最后输注后至少4周内超过4周。此类和其他研究表明,可能可以从两到四周的治疗间隔延伸。
在未来,治疗的个体化方法、仿制药的可得性和其他补体介导疾病的适应症的扩展可能会降低治疗成本,使患者更容易获得补体抑制。
进一步探索
2. Mele,C.,G. Remuzzi和M. Noris。2014.溶血性尿毒症综合征。Semin Immunopathol36: 399 - 420。
3.Davin, J. C.和n.c. van de Kar. 2015。补体介导的血栓性微血管病变管理的进展和挑战。其他副词内科杂志6: 171 - 185。
4.Ardissino, G., S. Testa, I. Possenti, F. Tel, F. Paglialonga, S. Salardi, S. Tedeschi, M. Belingheri和M. Cugno. 2014。非典型性溶血性尿毒症综合征的eculizumab维持治疗终止:10例报告。肾病64: 633 - 637。
5.Cugno, M, R. Gualtierotti, I. Possenti, S. Testa, F. Tel, S. Griffini, E. Grovetti, S. Tedeschi, S. Salardi, D. Cresseri, P. Messa,和G. Ardissino. 2014。监测非典型溶血性尿毒症患者eculizumab治疗的补体功能试验J Thromb Haemost12: 1440 - 1448。
6.Noris, M, M. Galbusera, S. Gastoldi, P. Macor, F. Banterla, E. Bresin, C. Tripodo, S. Bettoni, R. Donadelli, E. Valoti, F. Tedesco, A. Amore, R. Coppo, P. Ruggenenti, E. Gotti, G. Remuzzi. 2014。aHUS中补体激活的动态和如何监测eculizumab治疗。血124:1715-1726。
7.Volokhina, E. B., N. C. van de Kar, G. Bergseth, T. J. van der Velden, D. Westra, J. F. Wetzels, L. P. van den Heuvel和T. E. Mollnes. 2015。eculizumab治疗非典型溶血性尿毒症的敏感、可靠和易于执行的实验室监测。中国Immunol160: 237 - 243。
©2015医疗欧宝娱乐地址Xpress












用户评论