植物毒素致动物胆道闭锁
本周的一项研究科学转化医学是一个经典的例子,说明了看似不可能的合作者如何聚在一起做出令人惊讶的发现。一个由胃肠病学家、儿科医生、天然产物化学家和兽医组成的国际团队,通过研究斑马鱼模型和小鼠细胞培养,发现了澳大利亚植物中发现的一种化学物质,有助于了解影响新生儿的一种罕见的、使人衰弱的疾病的原因。这种疾病称为胆道闭锁(BA),是儿童肝移植最常见的指征。
研究小组分离出一种植物毒素,它具有一种以前未被描述的化学结构,可导致胆道闭锁在斑马鱼和哺乳动物的研究中,著名的合作者Michael Pack医学博士,胃肠病学部门和细胞与发育生物学部门的医学教授,以及Rebecca Wells医学博士,胃肠病学部门和病理与实验室医学系的医学副教授,都在宾夕法尼亚大学佩雷尔曼医学院。
BA是一种快速进展的破坏性疾病,影响肝外胆管内壁细胞。这条将胆汁从肝脏运送到小肠的大胆管内的细胞,由于一种尚未确定的环境伤害、毒素或感染而受损,导致瘢痕(纤维化)堵塞胆管,从而阻止胆汁流动。
BA的发病率为1/10,000至15,000活产。它发生在世界各地,是一种进展最快的肝硬化和肝硬化肝衰竭.幸运的是,婴儿可以使用一种挽救生命的治疗方法,一种叫做Kasai口肠造口术的外科手术,将一小段肠直接连接到肝脏,以恢复胆汁流动。然而,大多数婴儿最终会发展成肝硬化,并最终肝功能衰竭,导致在婴儿、儿童或青少年时期需要移植。

帕克和威尔斯与费城儿童医院弗雷德和苏珊娜·比塞克儿童肝脏中心的儿科胃肠病学家伊丽莎白·兰德医学博士和大卫·皮科利医学博士以及其他同事一起工作,他们对澳大利亚兽医报告的一种自然发生的BA模型产生了兴趣。在过去40年的极端干旱中,在不同寻常的牧场上放牧的羊和牛所生的后代都患有类似BA的综合征,与人类的BA基本相同。野外兽医史蒂夫·惠特克(BVSc)和兽医科学家彼得·温莎(Peter Windsor)博士(DVSc)在2007年的一次干旱中在羊羔中诊断出BA,他们将疫情与摄入了吞咽困难属植物(包括一种生长在正常水下土地上的叫做藜草的植物)有关,这表明动物BA是一种有毒的原因
“2007年的干旱一直持续到2008年,使我们能够从2007年事件中涉及的一个牧场上收获dyshania物种的植物,”Wells回忆道,她在2007年事件爆发后不久就与Whittaker联系,发起了合作,并安排将植物收获并进口到美国帕克补充说:“有了这种植物,我们知道我们有机会在实验室设计的斑马鱼生物测定法的指导下,确定负责的胆道毒素。”

合作者兼合著者John R. Porter博士是费城科学大学的一名天然产物化学家,他从植物中提取了粗提取物,在迭代过程中,Pack使用斑马鱼生物测定法将含有数千种化合物的混合物筛选到四种化合物的混合物。
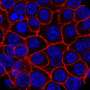
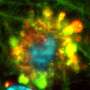
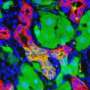
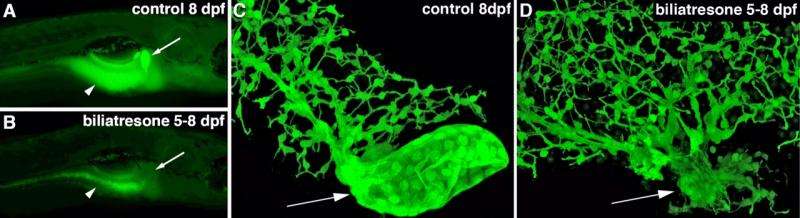
从这种混合物中,研究小组最终分离出了一种之前描述过的异黄酮,他们称之为胆酸resone。这种毒素使5岁大的斑马鱼幼虫产生BA,选择性地破坏胆管在肝外,但不在肝内。这种毒素对任何其他鱼类组织也没有明显影响,这与在人体BA中发现的结果类似。Wells的研究小组表明,植物毒素对哺乳动物细胞也有显著影响,引起胆管细胞结构和组织的变化,类似于受感染的人类胆管的变化。
这种毒素的一个令人费解的特性是它对大的肝外胆管的特异性。为了更好地理解为什么其他类型的肝细胞和较小的胆管没有受到影响,Pack检查了各种斑马鱼突变体,希望找到一种可能对胆管损伤更敏感或更抵抗的突变体。值得注意的是,他的团队能够识别出一个对毒素敏感的突变体,该突变映射到斑马鱼基因组中的一个区域,与之前的全基因组研究中发现的一个已建立的人类BA敏感性区域相似。这提供了进一步的证据,证明巴司尼亚综合征对理解人类巴司尼亚很重要。
帕克说:“总的来说,这些发现提供了直接证据,表明BA可能是由产前暴露于环境毒素引起的。”虽然很明显,人类没有食用与羊BA爆发有关的藜草或相关植物,但在甜菜、甜菜和其他消耗性植物中发现了一种与胆酸酮共同纯化的无毒、结构相关化合物。该团队目前正在研究肠道细菌是否能将这种活性化合物转化为活性毒素。
下一步,研究人员正试图合成足够数量的毒素,以研究其对小鼠的影响肝与鱼类相比,胆道系统与人类关系更密切。此外,帕克和威尔斯将利用他们在各自实验室中已经建立的模型来确定毒素的作用机制,并了解如何使用该模型来预防和治疗BA。
进一步探索