早期效益评估增加了研究数据的透明度
德国《药品市场改革法》(AMNOG)出台至今已有四年。AMNOG的主要目的是控制法定健康保险基金日益增加的药物支出。然而,AMNOG规定的新药早期疗效评估也揭示了迄今尚未发表的临床研究报告信息。来自德国卫生保健质量与效率研究所(IQWiG)的研究人员在发表在《德国医学杂志》上的一篇文章中进一步研究了这个问题英国医学杂志.
他们的结论:IQWiG进行的公司档案和档案评估,在早期效益评估期间发布新药,与其他公开的临床研究文件相比,包含了更多的信息,特别是在批准的亚人群中与患者相关的结果。药物的早期效益评估也可能适合作为其他国家或其他领域提高透明度的模式,例如评估非药物干预措施的效益
分析了22项研究的文献
IQWiG的研究人员共检查了15份包含22项临床研究的档案,以及IQWiG进行的相应档案评估。他们将这些文件与上述临床研究的常规文件进行了比较,即期刊出版物、研究登记条目和所谓的欧洲公共评估报告(epar),欧洲药品管理局(EMA)在其中提供了新药的证据。
他们评估了在每种类型的文件中,关于研究方法和结果的所有信息被完整报道的比例。该评价涉及已批准的患者群体,即产品特征摘要中规定的已接受新药治疗的患者。根据在药物批准过程中提交的研究中调查的所有患者组是否获得批准,或仅对其中一些组进行批准,要么分析研究总人群的信息,要么只分析已批准的亚人群的信息。然后将常规文件中信息的完整性与AMNOG文件(即公司档案和IQWiG的档案评估)进行比较。
更多关于批准的亚种群的知识
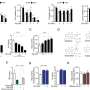
在分析研究总人群的情况下,传统文献中只有52%的研究结果被完全报道,而AMNOG文献中的相应比例为89%。在被批准的亚种群中,差异甚至更大。在与患者相关的结果方面,传统文献中的这一比例仅为5%,而AMNOG文献中的这一比例为70%。
IQWiG药物评估部门负责人Beate Wieseler解释说:“将我们档案评估中的词汇应用于AMNOG本身,而不是正在评估的药物:有迹象表明它有重大的额外益处。早期效益评估揭示了大量来自临床研究的额外信息:这对研究、医生和患者都是有益的,从而可以改善医疗保健。”
欧洲一体化不应危及进步
在他们的文章中英国医学杂志因此,作者建议在其他国家实施类似的法律规定。然而,在他们看来,德国还可以取得更多成就。例如,如果在这一领域也必须向卫生技术评估机构提交完整的研究报告,并且必须公布这些报告中的相关数据,就更容易确定非药物干预措施的益处。
该研究所所长Jürgen Windeler说:“今天关于新药的数据和文件没有消失在某个抽屉里,这不是制药公司自愿作出的自我承诺,而是法律的功劳。”“AMNOG还表明,临床研究报告几乎可以全部发表,而不会损害制药公司。”
现在德国应该保持透明度水平。欧洲目前正在讨论所谓的“联合评估”,即由几个HTA机构联合进行的效益评估。为此目的,必须商定共同的评估方法。但温德勒警告说:“这种协调不能是一种向下的调整。相反;AMNOG实现的透明度也应该成为其他欧洲国家的标准。”
更多信息:www.bmj.com/content/350/bmj.h796