科学家在一盘创建帕金森病
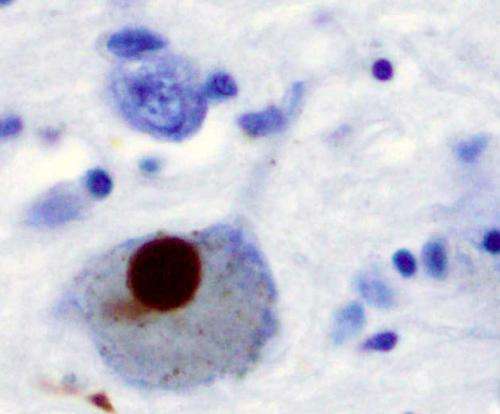
一组科学家领导的纽约干细胞基金会(NYSCF)研究所成功地创建了一个人类干细胞疾病模型的帕金森病。研究一对相同的同卵双胞胎,一个影响和一个与帕金森病的影响,另一个不相关的帕金森病人,和四个健康对照组,科学家们已经能够在实验室观察疾病的关键特性,明确不同病人的神经元的能力产生多巴胺,缺乏在帕金森病的分子。此外,科学家还发现了一个潜在的战略发展中帕金森氏症的新疗法。
归因于遗传和nongenetic因素的组合,帕金森病没有完全有效的治疗或治愈。帕金森病是适度遗传的,但这种继承的机制并不清楚。虽然遗传疾病的形式存在,零星的形式更常见。
“同卵双胞胎的独特的场景,一个与这种疾病和一个没有允许我们的科学家前所未有的研究帕金森病的机制,”苏珊·所罗门说,NYSCF首席执行官。“先进的干细胞研究技术允许我们推动科学的边界,看看出错在细胞水平上,一步一步在疾病过程中。”
DNA突变导致的生产特定的酶称为葡糖脑苷脂酶(GBA)与大了五倍患帕金森病的风险;然而,只有30%的人带有这种突变已被证明会在80岁患上帕金森症。这冲突表明,多种因素导致帕金森病的发展,包括基因和非基因因素。到目前为止,还没有合适的模型来识别和测试多个触发导致疾病的发生。
在这项研究中,在今天公布细胞的报道,一套同卵双胞胎,两个GBA突变,提供了一个独特的机会来评估和分析的遗传和非遗传贡献发展帕金森病在一个双胞胎,和缺乏病。科学家们由细胞诱导多能干细胞(iPS)从两个双胞胎的皮肤样本生成一个帕金森在培养皿的细胞模型,概括关键特性的疾病,特别是α-synuclein和多巴胺的积累不足。
在分析细胞模型,科学家们发现,从两个双胞胎产生多巴胺的神经细胞有GBA酶活性降低,α-synuclein蛋白水平升高,降低合成和释放多巴胺的能力。他影响哥哥相比,产生更少的多巴胺神经元产生的双重影响,有较高的酶单胺氧化酶B(缺氧),和穷人相互联系的能力。治疗分子,降低了活动的神经元缺氧与过表达GBA归一化α-核蛋白和多巴胺水平的细胞模型。这表明影响孪生的联合治疗可能通过同时针对这两个酶。
“帕金森病的主题不和谐的双胞胎给了我们一个令人难以置信的机会,利用干细胞疾病模型在培养皿中解锁一些疾病的生物机制,”斯科特Noggle博士说,NYSCF副总裁干细胞研究高级研究员和NYSCF——埃文斯阿尔茨海默氏症。“处理这些不同组织和科学家加入研究的深度和价值,我们希望我们的发现将适用于其他帕金森症患者和其他神经退行性疾病。”
在这个特定的场景中,基因和干细胞分析识别潜在有用的大道联合治疗的双重影响帕金森病和其他可能适用更广泛的帕金森患者。在这个案例研究中是独一无二的,这种类型的研究和细胞分析可能产生进一步的线索所有情况下的遗传和零星的帕金森氏症和其他相关的神经系统疾病。