新研究标识指导肠道神经元前体的迁移和分化的信号
神经发育涉及未成熟神经元的增殖和迁移,然后分化成化妆神经系统的多种细胞类型。这些过程较差,但已知需要数十种转录因子和信号分子的协调活性。Hideki Enomoto,Toshihiro Uesaka和来自Riken发展生物学中心的同事现已鉴定了一种控制肠道中大量神经元的迁移和分化的分子,称为肠溶神经系统(ENS)。
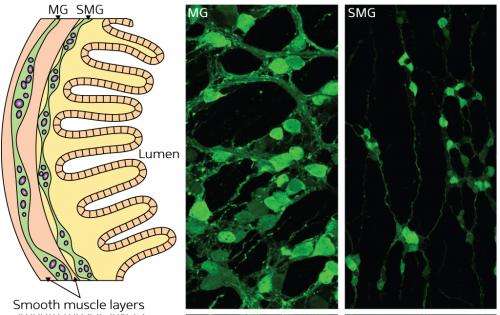
ENS(图1)由两个密集的神经元簇组成:神经元神经节(MG)和粘膜神经节(SMG)。它来自于神经嵴,沿着顶部产生的干细胞的瞬态群神经系统在早期发展。尽管大多数外周神经系统形式相对较快,但细胞迁移随后立即通过分化,形成SMG的ENA前体在很长一段时间内以不成熟状态被捕。
胶质细胞系衍生的神经营养因子(GDNF)需要过早的增殖和迁移来形成Mg。这些细胞仍然响应于稍后的发育阶段的GDNF,但到目前为止为什么不清楚。Uesaka和他的同事创造了一种遗传工程小鼠的菌株,其中编码GDNF受体的基因可以在任何时间点灭活并表达绿色荧光蛋白反而。
研究人员在EAR开发期间在各种时间点处丧失受体的表达,并在显微镜下跟踪标记的细胞。该研究表明,GDNF信号传导对于伯镁和次级SMG形成至关重要。他们发现保留在MG中的EnA前体表现出GDNF下游途径的最小活化。此外,缺乏GDNF受体的ENS前体维持其未分化状态。
结果表明,低水平的GDNF信号传导对于维持EAR前体中未分化状态的关键是至关重要的,并且GDNF对ENS - 前体迁移和神经元分化的动力产生长期影响。这在涉及GDNF受体再活化的实验中证实了这一点,这导致细胞恢复其迁移和神经元差异化。
“Hirschsprung的疾病与GDNF及其受体的基因有关,并且由GDNF调节的神经嵴干细胞功能可能有助于其发病机制,”Uesaka说。“了解调节前体 - 细胞维护的机制和神经元分化可以促进细胞更换策略的设计。“
进一步探索












用户评论