帕金森病在动物模型中停止
(欧宝娱乐地址医学快报)——数百万人患有帕金森氏症,这是一种影响运动的神经系统紊乱,随着时间的推移会恶化。随着世界人口老龄化,据估计,患有这种疾病的人数将急剧上升。然而,尽管有几种治疗帕金森症状的有效疗法,但没有什么能减缓其进展。
虽然目前还不清楚究竟是什么导致了这种疾病,但有证据指向了一个特定的罪魁祸首:一种名为α-突触核蛋白的蛋白质。这种蛋白质被发现在所有帕金森氏症患者中都很常见,当它“团块”或聚集在一起时,被认为是导致这种疾病的途径,并变得有毒,杀死大脑的神经元。
现在,加州大学洛杉矶分校的科学家们已经找到了一种方法来防止这些团块的形成,防止它们的毒性,甚至打破现有的聚集物。
加州大学洛杉矶分校神经学教授Jeff Bronstein和加州大学洛杉矶分校神经学副教授Gal Bitan及其同事报告了一种被称为“分子镊子”的新型化合物的开发,该化合物在活体动物模型中阻止α-突触核蛋白聚集物的形成,阻止聚集物的毒性,进一步逆转大脑中已经形成的聚集物。镊子在不干扰正常大脑功能的情况下完成了这一过程。
这项研究发表在该杂志的最新网络版上神经病治疗.
目前有30多种无法治愈的疾病是由蛋白质聚集及其对大脑或其他器官的毒性引起的,包括帕金森氏症、阿尔茨海默氏症和2型糖尿病。因此,布朗斯坦说,找到一种方法来阻止这种聚集过程是至关重要的。在过去的二十年里,研究人员和制药公司一直在尝试开发可以防止异常蛋白质聚集的药物,但到目前为止,他们几乎没有成功。
Bronstein说,虽然这些聚集物是药物的天然靶点,但找到一种只针对聚集物的治疗方法是一个复杂的过程。例如,在帕金森氏症中,与这种疾病有关的蛋白质α-突触核蛋白自然地遍布整个大脑。
布朗斯坦说:“它的正常功能尚不清楚,但它可能在帮助神经元之间的交流中发挥作用。”“那么,诀窍就是阻止α-突触核蛋白蛋白质聚集物及其毒性不会破坏α-突触核蛋白的正常功能,当然也不会破坏大脑的其他健康区域。
分子镊子
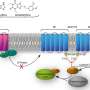
布朗斯坦与比坦合作,后者一直在使用他开发的一种名为CLR01的分子镊子。分子镊子是能够与其他蛋白质结合的复杂分子化合物。形状像字母“C”,这些化合物包裹着赖氨酸链,赖氨酸是一种基本氨基酸,是大多数蛋白质的组成部分。
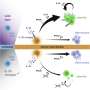
首先在细胞培养中工作,研究人员发现CLR01能够阻止α-突触核蛋白形成聚集物,防止毒性,甚至破坏现有的聚集物。
布朗斯坦说:“这项工作最令人惊讶的方面是,尽管这种化合物能够与许多蛋白质结合,但它对正常的、功能正常的脑细胞没有显示出毒性或副作用。”
“我们称这种独特的机制为‘过程特异性’,而不是常见的蛋白质特异性抑制,”Bitan补充道,这意味着该化合物只攻击目标聚集物,而不攻击其他东西。
接下来,研究人员在一种活的动物身上试验了他们的镊子,斑马鱼是一种水族馆中常见的热带淡水鱼。斑马鱼是一种受欢迎的研究动物,因为它很容易在基因上被操纵,发育迅速,而且是透明的,这使得生物过程的测量更容易。
利用转基因斑马鱼模型帕金森病,研究人员添加了CLR01,并使用荧光蛋白来跟踪镊子对聚集的影响。他们发现,就像在细胞培养中一样,CLR01阻止了α-突触核蛋白聚集和神经元死亡,从而在活体动物模型中阻止了疾病的发展。
能够阻止α-突触核蛋白聚集,防止毒性并破坏现有的聚集物是一个非常令人鼓舞的结果,但归根结底,“我们只是阻止了斑马鱼的帕金森症,”Bronstein说。
“尽管如此,”他说,“CLR01的所有这些好处都是在没有任何毒性证据的情况下发现的。综上所述,CLR01作为一种新药有望减缓或阻止帕金森病及相关疾病的进展。这让我们离治愈又近了一步。”
研究人员已经在帕金森氏症小鼠模型上研究CLR01,并表示他们希望这将导致人类临床试验。
这项研究的其他作者包括Shubhangi Prabhudesai、Sharmistha Sinha、Aida Attar、Aswani Kotagiri、Arthur G. Fitzmaurice、Ravi Lakshmanan、Magdalena I. Ivanova、Joseph A. Loo和Mark Stahl,他们都来自加州大学洛杉矶分校,以及德国杜伊斯堡-埃森大学的Frank-Gerrit Klärner和Thomas Schrader。