欧盟监管机构拒绝ALS病人药物激怒
欧盟药品监管机构拒绝批准一种肌萎缩性侧索硬化症药物已经批准在北美被称为“侮辱”愤怒的法国病人,谁说他们“没有时间等待”。
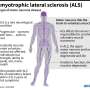
肌萎缩性脊髓侧索硬化症(ALS)也被称为卢伽雷的疾病无法治愈的神经退行性疾病,通常患者在三到五年的生活。
一种药物,利鲁唑,自1990年代以来已经存在和延长患者的生命大约三个月。否则,没有批准在欧洲新的治疗几十年了。
去年开发的新药叫AMX0035 Amylyx药品被考虑到绿灯在美国和加拿大。
欧洲药品局上周晚些时候表示,已拒绝授权的药物,具有欧美品牌Albrioza Relyvrio在美国。
EMA说2期临床试验的结果并不令人信服地表明,Albrioza有效减慢疾病的恶化。
“生存也不可靠的数据,数据收集和分析的方式,”该机构在一份声明中说。
法国ALS患者支持集团ARSLA说治疗是“唯一一个25年来带给我们希望通过展示放缓运动障碍由10个月和增加生存”。
美国公司已表示,将在欧洲再次申请批准。
但ARSLA表示,漫长的过程意味着EMA可能不会下统治在2024年10月之前发出。
“ALS患者没有时间等,”该集团表示。
第二阶段试验的基础是美国批准的137参与者。
Amylyx制药正在进行更大、更全面的第三阶段试验,结果预计将在2024年6月。
如果EMA正在等待结果,这意味着该药物可能不能批准在欧洲直到2025年,ARSLA说。
ALS攻击大脑和运动神经细胞脊髓逐渐麻痹肌肉,直到病人不能走路,吃饭,说话或呼吸。
在一个10000人的疾病在欧盟,根据教育津贴。
©2023法新社