阻止微小RNA可能防止老年性骨和肌肉损失,炎症

抑制的微小RNA水平显著增加随着年龄的增长,随着较弱的骨骼和肌肉松弛等问题,可能是一种方法,使我们的身体更年轻和健康,科学家说。
小分子核糖核酸帮助调节基因表达因此我们细胞的功能,和几个,其中一个叫微rna - 141 - 3 - p,已经与衰老的弊病,提高水平的潜在的破坏性慢性炎症和萎缩肌肉。
“当我们年龄在所有这些并发症慢性炎症,肌肉损失,骨损失,这种微高,”Sadanand说Fulzele,兽医学博士博士,衰老的医学研究员乔治亚州奥古斯塔大学的医学院。“我们想要压制它。”
在什么似乎是第一个研究,Fulzele和他的同事使用一种抑制剂他专门设计的,能阻挡微rna - 141岁3 - p老鼠。这些类型的工程分子被称为antagomirs,虽然目前限于研究,有一天治疗价值Fulzele说,病人研究的通讯作者衰老和疾病。
老鼠,相当于人类60年代,是治疗三个月每周antagomir皮下注射,一个方案,可以很容易地用于人类。
科学家们然后看着血液中发生变化,脾脏,其任务包括调节水平的对抗白细胞,以及骨骼和肌肉。他们发现到处都看起来更年轻的概要文件。
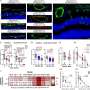
在脾脏,例如,他们看到更多的inflammation-reducing免疫细胞被称为巨噬细胞(M2)而不是他们有助改善炎症与物损伤你的心脏(M1)。m2也已报告支持组织修复。有助改善炎症蛋白质物损伤你的心脏血液水平较低的被称为细胞因子,和骨的微观结构更加稳固和肌肉纤维尺寸大。
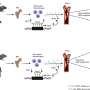
他们发现,微RNA - 141 - 3 - p调节AUF1的表情,“好”基因的工作很多,包括调节稳定性的信使RNA, DNA蛋白质发挥作用的最终。AUF1有助于保护年轻人从制造如此多的促炎的il - 6等产品,导致慢性破坏性炎症。它同样细胞衰老时细胞变得不那么能够正常运转和分裂但通常不会死。更高水平的微rna - 141 - 3 - p意味着更少的保护AUF1和阻断微启用更高水平,从而减少炎症和衰老。
Fulzele指出,像其他所有的身体,微rna - 141 - 3 - p的影响和其老化的表达和水平高。他们最新的发现指出了减少其表达式作为一个可能的策略来提高免疫,骨骼和肌肉健康随着年龄的增长,Fulzele说。
水平的炎症和氧化应激在任何年龄是整体健康的指标。慢性炎症和慢性氧化应激的标志是一个衰老的身体和重要球员消极的变化结果。
随着年龄的增长,细胞的修理/更换能力被降低,这样,例如,骨质流失开始超过新骨形成。同时炎症,愈合的要素,但是在慢性破坏性,高水平,向上蔓延。产生的问题的范围可以从增加身体虚弱等疾病的发病率增加癌症、心血管疾病和老年痴呆症。
Fulzele指出,他的研究是面向设法防止伤害,而不是试图恢复一个健康正常的。他的下一个步骤包括观察阻断微如何影响其他与年龄相关的问题,如认知和给微- 141 - 3 - p -具体antagomir更长的时间。他说他们没有识别出任何明显的副作用超过三个月的研究。
Fulzele和他的同事们发表在2018年的证据表明,随着年龄的增长,微rna - 141 - 3 - p的表达上升时的关键信号分子基质细胞衍生因子1,或SDF-1,帮助干细胞使健康的骨骼和肌肉,向下负责的间充质干细胞使骨骼和肌肉和脂肪。SDF-1帮助调节分化为不同的细胞类型。在人类和老鼠间充质干细胞科学家发现微rna - 141 - 3 - p水平较低的年轻细胞,在老细胞的三倍或更高。SDF-1水平细胞直接相反。随着年龄的增长,间充质干细胞也让更多的脂肪,而不是骨骼或肌肉,它们倾向于因为脂肪更容易做。
更多信息:抑制微rna - 141 - 3 - p改善老年小鼠肌肉骨骼健康,衰老和疾病(2023)。DOI: 10.14336 / AD.2023.0310-1。www.aginganddisease.org/EN/10.14336/AD.2023.0310-1