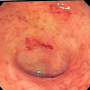
小干扰rna作为体内自组装形态联合治疗溃疡性结肠炎
尽管最近我们的知识进步的溃疡性结肠炎的致病机制,仍有相当大的未满足的医疗需要治疗的条件。
因为溃疡性结肠炎是一个多因素,多步骤的过程,仅仅阻止单个炎性细胞因子或免疫目标可能不是足够治愈这种疾病。联合治疗溃疡性结肠炎的针对多个致病基因和通路可能是必需的。
不幸的是,目前的治疗方法通常是基于独立的化合物或单克隆抗体,联合治疗的潜能尚未意识到治疗溃疡性结肠炎。
由于高特异性、力量和灵活性的小干扰rna (siRNAs) cotarget多个基因在单一剂量,siRNA-based疗法提供一个有吸引力的战略联合治疗溃疡性结肠炎。然而,一个适当的体内输送系统的开发siRNAs仍然RNAi疗法的主要瓶颈。
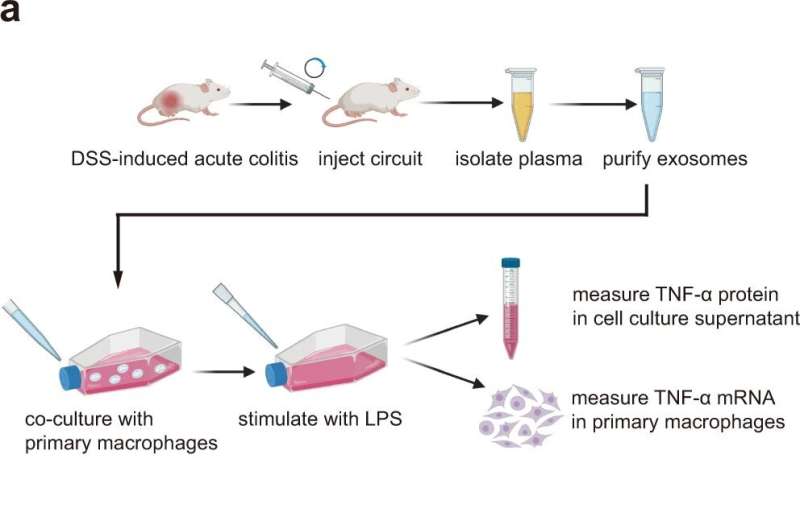
在一项新的研究发表在自然通讯教授领导的联合研究小组,Chen yu, Xi陈和张Qipeng南京大学开发出一种合成生物学相结合的策略存在的自然循环系统的小细胞外囊泡与人工基因电路重组雄性老鼠的肝脏多个siRNAs自组装到小细胞外囊泡分泌和促进体内交付siRNAs通过循环小细胞外囊泡的联合治疗溃疡性结肠炎的小鼠模型。
特别是重复插入多靶向基因电路设计的同时抑制TNF-α,B7-1和整合素α4迅速缓解肠道炎症和产生了协同治疗效果通过抑制促炎症级联对溃疡性结肠炎结肠巨噬细胞,抑制costimulatory信号T细胞,阻断T细胞归巢的炎症。
更重要的是,他们设计了一个AAV-driven基因电路引入TNF-α的实质性的和持久的抑制,B7-1和整合素α4只通过一个注入。总的来说,本研究建立了一个可行的治疗溃疡性结肠炎的策略组合,这可能提供了一个替代传统生物疗法需要两个或两个以上独立的化合物或抗体。
这项研究很重要,因为以下原因:
(1)多目标遗传电路形成裸DNA质粒或AAV和简单的管理静脉注射;然后,多个siRNAs自发产生的,同时肝脏和转移通过小细胞外囊泡的循环系统。这个设计借用人体自身的小RNA装配和运输机械和重新构建联合治疗的策略,从而解决的瓶颈问题联合治疗溃疡性结肠炎。
(2)体内蛋白自组装siRNA减轻溃疡性结肠炎的症状特点更好的程度上作为TNF-α抗体英夫利昔单抗。由于单克隆抗体遭受一些固有的局限性抗体药物(如高成本,严重的副作用和代anti-antibodies)体内蛋白自组装siRNA持有强烈的承诺成为患者的新选项溃疡性结肠炎。
(3)本研究提供了基础交付siRNAs网站和发炎免疫细胞调节免疫反应。因为过度的免疫反应是许多自身免疫性疾病的标志,体内蛋白自组装siRNA有望加快发展的新疗法自身免疫性疾病(例如,系统性红斑狼疮和类风湿性关节炎)。
更多信息:苑周et al,体内小干扰rna作为自组装形态联合治疗溃疡性结肠炎,自然通讯(2022)。DOI: 10.1038 / s41467 - 022 - 33436 - 0