调查哥伦比亚神经退行性疾病背后的罕见突变
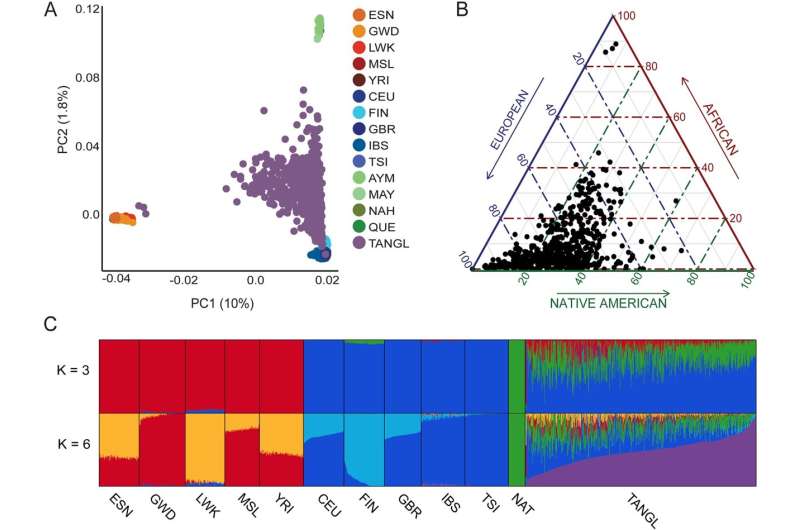
30年前,加州大学圣巴巴拉分校(UC Santa Barbara)神经科学家肯尼思·s·科西克(Kenneth S. Kosik)首先开始研究一个哥伦比亚家庭,这个家庭患有一种遗传形式的早发性阿尔茨海默病。他和其他研究人员意识到,他们只是触及了西班牙近五个世纪前殖民所造成的基本上看不见但却深远的后果的表面。
“当我的同事在这个携带这种突变的庞大农村家庭的个体上进行临床试验时,他们需要尽可能多的参与者,”Kosik回忆起为这项研究招募人员所做的努力。这个由几千人组成的家庭是独一无二的。携带所谓的Paisa突变基因的人会像时钟一样,在40多岁时开始出现阿尔茨海默氏症的标志性健忘——他们称之为la bobera。
研究人员与哥伦比亚神经科学家弗朗西斯科·洛佩拉(Francisco Lopera)合作,试图尽可能广泛地撒网,即使是在该国偏远地区也能找到那些患有早发性痴呆症的人,这些人在哥伦比亚造成了如此多的不必要的痛苦。
这种情况的严重程度远远超出了他们的预期——他们的调查得出了可以追溯到几千年前,横跨几个大陆的基因结果。研究人员的研究成果发表在该杂志上基因组医学.
遥远的起源
Juliana Acosta-Uribe还记得这项研究的早期情况。当时,她是一名医科学生,即将结束学业,成为一名内科科学家,并投入了一年的社会服务。
“我们接到了1000多个家庭中患有早发性痴呆症的人的电话,”Acosta-Uribe说,他现在是Kosik实验室的项目科学家,也是这篇论文的主要作者。“我们正在测试它们,看看它们是否属于携带派萨基因突变的家族。”
但当他们测试这些人的PSEN1 E280突变时,研究人员认为他们的新患者在某种程度上是原始家族的一个子集的假设消失了。绝大多数检测结果呈阴性。进一步的测试表明,研究人员集中了一些不相关的、具有不同基因的家族突变这导致了相同的可观察特征。
“我们已经很擅长识别导致疾病的不同突变神经退行性疾病-他们的基因型,”Kosik说。“但我们并不真正了解基因型和他们的表型之间的关系,也就是说,他们在临床上看起来是什么样子,他们得的是什么类型的痴呆症,它是如何发生的,什么机制受到影响。”
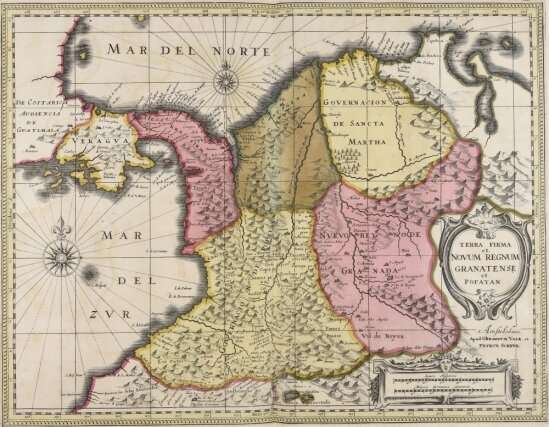
基因组测试只揭示了这个故事的一部分,最初的信息似乎只会加深谜团。例如,著名的派萨突变可以追溯到西班牙哈布斯堡王朝早期的一位创始人,而另一种突变则可以追溯到西非。还有一种被认为具有美洲原住民的血统。它们是如何出现在哥伦比亚的农村地区的?
这一现象的线索可以在哥伦比亚的历史和全球范围内的人口流动中找到。
阿科斯塔-乌里韦说:“人口统计学、人口历史和人口流动的许多不同因素形成了目前阿尔茨海默病的风险负担。”在西班牙征服美洲期间,16世纪初,欧洲人首次出现在后来成为哥伦比亚的北部海岸,努力在该地区定居和殖民。在那个世纪后期,西非人也成为了被奴役的劳工。
然而,当时在哥伦比亚,人们并不是唯一的混血儿。
阿科斯塔-乌里韦说:“人们不会独自旅行。“人们带着虫子旅行。”根据研究人员的说法,这些人与以前从未见过它们的人交换它们,人们“因各种传染病而大量死亡,包括天花、流感、梅毒、肝炎、麻疹、脑炎、结核病、白喉、霍乱、斑疹伤寒、猩红热和脑膜炎”。
种群的崩溃导致了基因库的缩小,这是一个遗传瓶颈,在这个瓶颈中,剩下的少数幸存者碰巧也拥有这些罕见的突变,他们成为了随后种群的创始人,将他们的突变遗传给他们的后代。随后是一段漫长的殖民时期,移民速度放缓,人们大多呆在原地。缺乏新基因、孤立的人群和大家庭有助于在人群中建立突变。
Kosik解释说:“如果他们有几代人的大家庭,这些突变就会被放大,而且是在局部放大,因为人们没有四处流动。”“我们在哥伦比亚开始看到的是,基因图谱与地理图谱重叠,因为你实际上可以将基因突变的人与某个地区匹配。”
这一机制解释了突变如何能够在种群中增殖。但研究人员的调查引发了另一个问题,一个难以忽视的问题。
“当你给一个群体施加选择性压力时,比如病原体,随之而来的问题是,幸存者比死者有什么好处吗?”Acosta-Uribe说。这些突变——特别是PSEN1(早老素)基因的变异——是否在早期的殖民时期赋予了携带者某种保护,使其免受传染病的侵袭,从而确保了他们的生存?
阿科斯塔-乌里韦说,这种情况并不罕见。
她说:“有很多例子表明,有基因变异的人在其他情况下可能是有害的。”例如,她指出,患有镰状细胞贫血症的人杂合(来自父母一方的一个突变基因副本和来自父母另一方的一个正常副本)对严重疟疾有抵抗力。导致镰状细胞的突变也“干扰了疟原虫的繁殖周期”。
Kosik说,不幸的是,有这些PSEN1突变帮助他们的携带者抵御致命传染病的概念可能永远处于推测的领域。
他说:“我们无法重放人生的录像。”“我们无法回放发生在那里的一切来证明这一点,但这是相当可信的。”在这个谜题中有两个诱人的旁证:仅在哥伦比亚队列中就发现了13个PSEN1基因突变(对于哥伦比亚这样一个面积和人口众多的国家来说,这些罕见突变的浓度“在统计学上是不寻常的”),以及导致阿尔茨海默病特征——粘性不溶斑块的多肽的抗菌特性。
“事实证明,淀粉样β肽可能具有抗菌功能;这是一种非常古老的防御入侵生物的系统,其中一种抗菌肽附着在入侵生物上,并将其与身体的其他部分隔离开来,”Kosik说。据推测,这种特殊的突变可能被积极选择,也许是因为它可以保护人们免受疾病的侵害。Kosik补充说,他的实验室正在研究这种影响,对他们队列中的基因组进行更深入的研究,但这充其量可能只是一个统计上的争论。
随着Kosik实验室继续工作,一项重大临床试验的结果即将出炉,很明显,他们生成的庞大基因组数据集只是全球人群疾病遗传学的冰山一角。
阿科斯塔-乌里韦说:“我们已经生成了一个独特的数据集,可以帮助我们了解非白人人群疾病的遗传。”她补充说,大多数基因组数据集中在欧洲基因组上,当涉及到人类基因相关疾病时,这可能会掩盖大部分情况。突变和其物理结果之间的联系尤其如此。
例如,阿科斯塔-乌里韦在为这个项目进行的基因组调查中发现,在欧洲出现的ALS(也称为卢伽雷氏病)的突变和病理在美洲原住民谱系中出现的是额颞叶痴呆。此外,通过追溯印第安人突变的时间,她发现它起源于美洲的第一批人口。
阿科斯塔-乌里韦说:“我们将携带这些变体的哥伦比亚人与携带这种变体的亚洲人进行了比较,我们发现,哥伦比亚人确实从他们的祖先那里得到了这种变体,他们在3万多年前穿越白令海峡迁徙到美洲。”
回到现在,这个新知识可以为哥伦比亚队列的成员提供一些线索,为什么阿尔茨海默病的遗传形式在他们的家庭中如此普遍。它还强调了在努力了解和可能治疗这种尚未治愈的疾病方面进行合作的价值。一个亮点是:家族中有一位携带派萨基因突变的女性终其一生都没有患上阿尔茨海默氏症,这可能是因为这种罕见基因突变的第二个副本分离了这种疾病的两个标志性迹象:淀粉样斑块(在她死后在她的大脑中被发现)和tau蛋白缠结(未被发现)。
Acosta-Uribe说:“这篇论文使我们与科学界和哥伦比亚的家属建立了紧密的联系。”“我们能够向家属解释为什么会发生这种事,并告诉他们,虽然我们可能还不能治愈他们,但我们会和他们在一起。”
更多信息:Juliana Acosta-Uribe等人,由于创始人效应,哥伦比亚罕见突变的神经退行性疾病景观,基因组医学(2022)。DOI: 10.1186 / s13073 - 022 - 01035 - 9