一项开创性的研究发现了婴儿痉挛的潜在原因,并指出了一种新的治疗方法
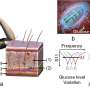
婴儿痉挛(IS)是一种严重的婴儿癫痫综合征,占婴儿出生一年内发生的所有癫痫病例的50%。目前对这种疾病的治疗选择有限,大多数受影响的婴儿长大后会出现发育迟缓、智力障碍和其他类型的严重癫痫。戈登和玛丽·凯恩儿童神经学研究基金会实验室主任、德克萨斯儿童医院简和丹·邓肯神经学研究所研究员、贝勒医学院教授约翰·斯万博士的实验室进行的一项开创性研究发现,在IS患者和动物模型的大脑中,胰岛素生长因子-1 (IGF-1)及其下游信号的水平都降低了。此外,他们发现给IS动物模型注射IGF-1类似物成功地消除了痉挛和异常大脑活动。这项令人兴奋的研究发表在神经病学年鉴这项技术有可能改变婴儿痉挛的治疗现状。
斯万博士是癫痫研究的领先专家,几年前,他的团队的开创性发现导致fda批准治疗结节性硬化症患者的严重癫痫。他和他的团队对研究有着长期的兴趣和经验婴儿痉挛症在美国,每年大约有2500名婴儿被诊断出癫痫。
早期脑损伤会降低IGF-1水平,损害IGF-1信号通路
“此前有报道称,患有大脑异常的IS患者的大脑中IGF-1水平较低脑脊髓液基于此研究斯旺说:“在美国,我们有兴趣调查IS动物和患者大脑中的IGF-1水平是否发生了变化。”
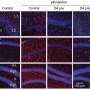
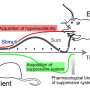
在他们的研究中,研究小组使用了一种成熟的方法来诱导啮齿动物自发的癫痫痉挛。该方法于2008年在Swann实验室开发,包括将河豚毒素(TTX)长期输注到幼鼠大脑皮层,这会在输注部位造成损伤,并导致与IS患者几乎相同的痉挛。
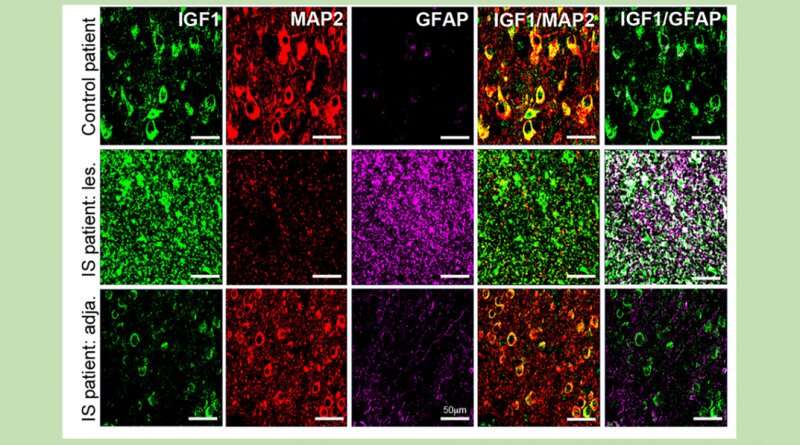
正如人们所期望的那样脑损伤,我们发现TTX输注部位的非神经元支持细胞(又名胶质细胞)中IGF-1水平升高。然而,我们最感兴趣的是IGF-1表达的显著和广泛的下降大脑皮层神经元在大脑区域靠近或远离TTX注射部位,这是一种以前从未报道过的现象,”Swann说。
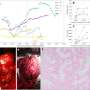
接下来,研究小组研究了患有围产期中风并接受手术控制顽固性癫痫的IS患者的切除的皮质组织。结果与他们在IS动物身上看到的结果惊人地相似。
“更重要的是,我们发现IGF-1皮质水平的降低在IS动物模型中有显著的影响,因为它抑制了IGF-1分子信号通路的整体活性,这些信号通路调节了早期大脑发育和神经元功能中许多重要的生物过程,”斯旺实验室的博士后副教授、该研究的第一作者卡洛斯·巴雷斯特-罗萨多博士说。
IGF-1类似物可以消除动物的婴儿痉挛
为了确定增加IS动物皮层中的IGF-1水平是否可以改善痉挛,研究小组使用了一种较小版本的IGF-1,它可以比全长激素更容易穿过血脑屏障。他们测试的IGF-1三肽是正常情况下在大脑中发现的IGF-1分解的自然副产物。此外,这种类似物先前已被证明可以成功逆转其他神经发育障碍(如Rett综合征和Phelan-McDermid综合征)动物模型中的行为缺陷。
Swann说:“利用几条证据,我们首先证实了这种IGF-1三肽能够激活小鼠体内的IGF-1信号级联。”“然后我们惊讶地发现,注射IGF-1成功地消除了痉挛和is特异性混乱大脑在大多数IS动物中,这种活动模式被称为轻度心律失常。我们很兴奋,因为这些发现提出了一种诱人的可能性,即这种IGF-1类似物未来可以用于治疗IS患者。”