一种新的渐冻症和痴呆症发病机制的发现提高了治疗的希望
由伦敦大学学院(UCL)和国立卫生研究院(NIH)的科学家领导的一项开创性的新研究首次揭示了为什么一种常见的遗传变异会恶化患有毁灭性的成人神经退行性疾病肌萎缩性侧索硬化症(ALS)和额颞叶痴呆(FTD)的人的疾病结局。
发表在自然,该研究显示了与几乎所有(97%)ALS病例和一半FTD病例相关的TDP-43蛋白损耗如何破坏关键神经元蛋白UNC13A的遗传指令。
引人注目的是,它发现了一种神秘的基因变异疾病风险增加了《UNC13A》基因指令在疾病患者中被破坏的机会,从而恶化了ALS和FTD的风险和严重程度。
UNC13A使神经元(神经细胞)能够通过神经递质释放相互交流,来自动物模型的数据表明,神经元失去UNC13A可能是致命的。研究人员认为,UNC13A基因指令在患者身上的破坏可能会产生类似的有害后果。
渐冻症是最常见的运动神经元疾病,目前尚无治愈方法;它通过攻击控制运动的神经元和神经来影响大脑和脊髓,导致它们死亡。目前,英国只有一种被批准的治疗ALS的药物,它可以延长几个月的寿命,而且只对极少数患者有效。三分之一的患者在确诊后的一年内死亡。
FTD是一种潜在病因相似的相关疾病;症状包括语言障碍、性格改变和认知困难。
研究人员表示,这一发现为新疗法带来了希望;通过开发一种疗法来阻止《联合国13a公约》的腐败遗传指令在美国,大多数ALS患者和大约一半的FTD患者的疾病进展可以减缓。
通讯作者Pietro Fratta教授(伦敦大学学院皇后广场神经学研究所)说:“大多数研究基因治疗一直关注与家族性肌萎缩性侧索硬化症(有家族病史的患者)相关的基因,但绝大多数ALS病例是散发的,没有已知的家族病史。”
共同通讯作者Michael Ward博士(美国国立卫生研究院国家神经疾病和中风研究所)补充说:“我们早就知道UNC13A基因变异会增加ALS和痴呆的风险,但没有人弄清楚为什么会这样。我们的团队共同展示了这种导致ALS的遗传风险因素如何与核心疾病机制TDP-43缺失相互作用,从而恶化疾病进程。”
tdp -43 - ALS和FTD的关键分子
可以说,在渐冻症研究中最重要的蛋白质是TDP-43,在大多数情况下(以及一半的FTD病例),这种蛋白质是不正确地从细胞核中弹出的。这阻止了TDP-43发挥其重要功能,例如确保mRNA的正确产生。
沃德博士说:“我们早就知道,大多数ALS患者和大约一半的FTD患者失去了一种叫做TDP-43的关键蛋白质的功能,对大脑造成了严重破坏神经细胞都受到了影响。但我们还不知道如何扭转TDP-43损失带来的最严重后果。”
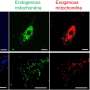
作为实验研究的一部分,研究人员使用皮肤来源的人类干细胞在培养皿中制造神经元细胞,并使用基于CRISPR-Cas9(诺贝尔奖得主基因编辑技术)的新技术从这些细胞中去除TDP-43蛋白。
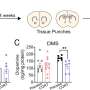
然后,科学家们能够研究这些没有TDP-43的神经元与健康神经元的区别。他们发现UNC13A蛋白的mrna被破坏了,这意味着实验室培养的神经元中的核糖体无法正确地产生UNC13A蛋白。此外,当研究小组观察ALS和FTD患者的大脑样本时,他们再次发现UNC13A的mrna是不正确的,这证实了他们的实验复制了现实世界的疾病过程。
鉴于UNC13A在促进神经元通信方面发挥的重要作用,因此它的破坏可能损害神经元功能,并导致ALS和FTD患者的神经退行性变。
遗传变异增加了UNC13A mRNA腐败的风险
UNC13A基因及其对应的蛋白质长期以来一直是运动神经元疾病和FTD研究人员的兴趣点,之前的研究表明,常见的遗传变异会增加疾病的风险和严重程度,尽管在大多数未受疾病影响的人身上是良性的(一半的人口携带其中一种变异,只对ALS或FTD患者有害)。然而,尽管经过了十多年的研究,其确切原因仍然是神秘的,因为这些变体并不直接改变UNC13A蛋白编码序列,而是位于“垃圾DNA”区域。
研究人员认为,他们已经找到了这个关键问题的答案:他们发现,一旦ALS和FTD疾病进程开始,风险相关的变异极大地增加了UNC13A mRNA被破坏的机会,以及相关的TDP-43蛋白的损失。因此,具有这些遗传变异的患者可能遭受更大的UNC13A损失,从而导致更严重的疾病。
该研究的共同主要作者、博士生奥斯卡·威尔金斯(伦敦大学学院皇后广场神经学研究所和弗朗西斯·克里克研究所)说:“这些结果代表了一个重大突破,原因有几个。首先,它们解释了为什么UNC13A基因变异会增加运动神经元疾病和痴呆症的风险,这是一个困扰研究人员十多年的问题。他们也首次证明了核TDP-43功能丧失与ALS之间的遗传联系,提高了对这种核心疾病机制的科学理解。”
下一个步骤
Fratta教授说:“我们在多年的遗传研究的基础上确定了UNC13A与运动神经元疾病和FTD有关,并以一项新的分子生物学发现来支持这一研究,该发现证实了该基因绝对是疾病过程的基础。
“我们希望在未来几年进行试验,开发出这样一种治疗方法,可能会极大地改善ALS患者的生活。”
研究人员相信,有了这些新信息,可以创造出治疗运动神经元疾病的新疗法,阻止UNC13A mrna在患者体内被破坏。
这项研究涉及伦敦大学学院、美国国立卫生研究院、克里克、纽约基因组中心、西奈山、国际基因工程和生物技术中心以及国家化学研究所(斯洛文尼亚)的研究人员。这项研究由医学研究委员会、运动神经元疾病协会和美国国立卫ob欧宝直播nba生研究院资助,并得到玫瑰树信托基金、罗伯特帕卡德ALS研究中心、威康、应用纳米技术合作中心和x -联性肌张力障碍-帕金森症合作中心的支持。
更多信息:TDP-43缺失和als风险snp驱动UNC13A错剪接和损耗,自然(2022)。DOI: 10.1038 / s41586 - 022 - 04436 - 3,www.nature.com/articles/s41586 - 022 - 04436 - 3