τ和PQBP1:蛋白质相互作用诱发炎症在大脑中
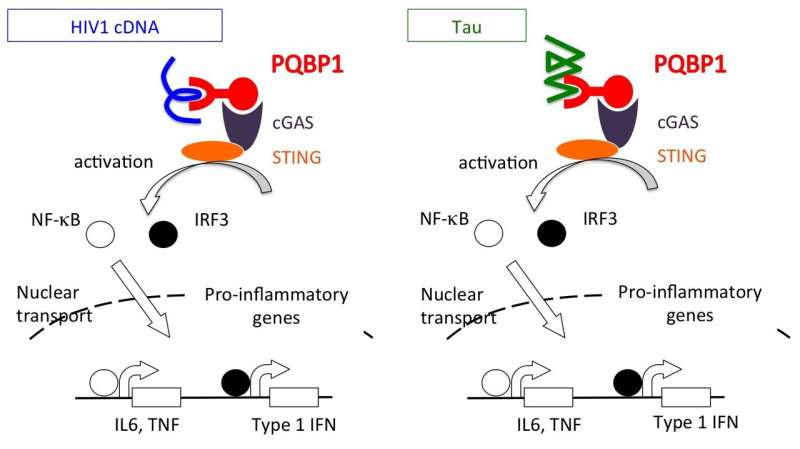
就像一个家庭安全系统可以提醒房主入侵者的存在,受到多麸醯胺酸蛋白结合蛋白1 (PQBP1)中发现脑细胞可以提醒身体“入侵”病毒的存在就像人类免疫缺陷病毒(HIV)。现在,日本的研究人员揭示PQBP1的角色失调与神经退行性疾病相关的蛋白质的检测。
在一项新的研究发表在自然通讯,研究人员从东京医疗和牙科大学(TMDU)揭示了细胞内受体的作用PQBP1τ,蛋白质主要发现在神经元中发挥着关键作用在神经退行性疾病如阿尔茨海默氏病的发展。
PQBP1已被证明有意义和绑定艾滋病毒DNA和引发免疫途径称为cGAS-STING途径启动炎症反应。虽然PQBP1也被证明与那些牵涉等不正常的蛋白质神经退行性疾病亨廷顿氏舞蹈症,具体PQBP1在神经退行性炎症反应中的作用还不清楚。为了更好地理解这种关系,研究人员从TMDU着手阐明PQBP1之间的相互作用的性质和τ。
描述PQBP1之间的关系和τ,我们能够澄清的大脑炎症的机制功能在病毒感染和神经退行性疾病,”说,这项研究的资深作者,仁Okazawa。
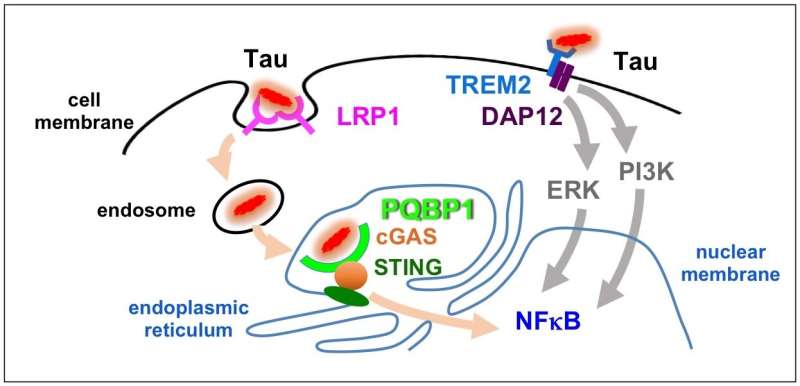
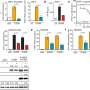
研究者使用小胶质细胞,进行体外分析PQBP1-expressing免疫细胞在大脑中发现,证明τ与PQBP1交互,这种交互驱动通过cGAS-STING通路的激活免疫反应。他们的研究显示,PQBP1-cGAS-STING通路功能与TREM2-mediated通路,其突变与阿尔茨海默病的基因。
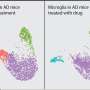
他们继续使用鼠标模型PQBP1被有条件地灭活在小胶质细胞表明表达PQBP1 Tau-induced炎症反应体内是必要的。
“我们很高兴发现在小胶质细胞灭活PQBP1小鼠模型减少脑部炎症为了应对注入τ进入大脑,”Okazawa说。
研究小组还发现,突变τPQBP1-binding地区减少了炎症的发生大脑为了应对τ注入。这些发现表明,PQBP1可能代表一个潜在的目标发展的疗法Tau-mediated神经退行性疾病的治疗。
更多信息:美华金et al,τ激活小胶质细胞通过PQBP1-cGAS-STING途径促进脑部炎症,自然通讯(2021)。DOI: 10.1038 / s41467 - 021 - 26851 - 2