囊性纤维化在人类肺气道芯片上忠实地建模
遗传性进行性疾病囊性纤维化(CF)通过影响产生粘液、汗液和消化液的细胞,对肺和身体其他组织造成严重损害。囊性纤维化跨膜电导调节基因(CFTR)编码离子通道,控制离子和水在细胞内外的流动。在携带CFTR基因突变的个体中,气道和其他通道中的黏液,通常是薄而滑的,变得粘稠——因此,它不是作为润滑剂,而是成为充血剂。
患者筛查和突破性疗法的进步使CF患者现在可以活到30多岁或40多岁,有时甚至更长。然而,即使是约90%的CFTR突变患者(依赖于大陆),被称为ΔF508,可以用现有药物治疗,仍然受到细菌在粘液中沉积的困扰,导致肺部炎症。感染和炎症的反复发作,以及感染之间的慢性低级别炎症,会逐渐削弱并损伤患者的气道,最终导致他们的呼吸系统衰竭。对于其余约10%的CFTR突变患者,甚至还没有靶向治疗方法。开发新的迫切需要的治疗方法的一个主要障碍是缺乏概括CF疾病病理的人体体外模型。
现在,哈佛大学Wyss生物工程研究所的一个多学科研究小组在Wyss创始主任Donald Ingber博士的领导下,在囊性纤维化基金会的资助下,开发了一种USB记忆棒大小的微流体器官芯片设备,它比迄今为止的其他体外系统更准确地总结了CF患者的关键病理特征。该模型复制了该疾病多种特征的cf特异性变化,包括气道黏液层、输送黏液的纤毛跳动、病原体生长、炎性分子以及白细胞的补充细胞,为研究新的CF疗法提供了一个全面的临床前人类模型。研究结果发表在囊性纤维化杂志.
“现在我们能够准确地模拟CF病理,包括微生物组和炎症反应在人类气道芯片中,我们有一种方法来应对对CF患者很重要的挑战,”Ingber说。“这种先进体外模型的捆绑功能可以帮助加速寻找可能抑制夸大的药物免疫反应在患者中,用更个性化的疗法来治疗他们,并帮助解决CF患者每天面临的现有疗法无法解决的问题。”Ingber还是Wyss生物启发治疗和诊断平台的教师领导,也是哈佛医学院和波士顿儿童医院的Judah Folkman血管生物学教授,以及哈佛大学约翰·a·保尔森工程与应用科学学院的生物工程教授。
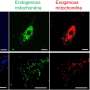
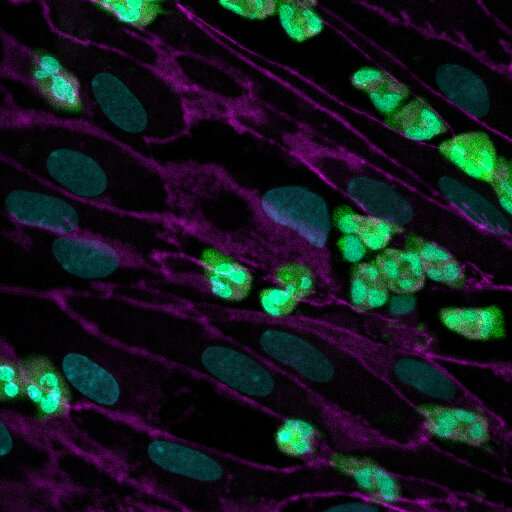
为了模拟和比较血管化的CF气道的微观结构和功能,作者从人类CF患者或健康个体中获得肺气道细胞,在空气下的微流控设备的两个平行运行的空心通道之一中生长,概括了肺的空气运输环境。在第二个通道中,通过多孔膜与第一个通道分开,他们用灌注血液替代介质的人类肺微血管细胞重新创造了一个人类血管。
“这是CF气道的第一个微生理模型,与我们对CF患者气道的了解非常相似。它保持了所有相关细胞类型的典型组成,形成了更厚的黏液层,它的纤毛细胞表现出更高密度的纤毛,与健康个体的气道细胞形成的气道芯片相比,它们的搏动频率更高,”Ingber团队的共同第一作者、前博士后Ratnakar Potla说。“重要的是,这些病理变化伴随着模拟CF支气管上皮炎症反应的增强,这与在CF患者中观察到的非常相似。”Potla现在是基因泰克-罗氏公司体外系统复合体的高级科学家。
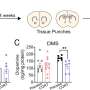
在培养气道芯片两周后,研究人员测量了气道芯片血管通道中流出的促炎因子和抗炎因子的水平,这些因子已知与CF患者肺部的炎症反应有关。在其他变化中,与对照组气道芯片相比,CF芯片中的促炎细胞因子IL-8水平增加。有趣的是,IL-8以其吸引中性粒细胞的能力而闻名,中性粒细胞也会导致CF患者肺部的炎症。
当研究人员将人体中性粒细胞通过CF气道芯片的血管通道时,他们观察到更多的免疫细胞自发地粘附在血管细胞表面,通过血管细胞层和多孔膜挤压自己,并积聚在气道的气道上皮细胞层,这一过程被称为“转生”。
但模仿cf的气道组织不仅刺激了免疫细胞的募集,还支持了细菌的生长,铜绿假单胞菌,它存在于正常肺部的微生物组中,但可以生长失控,导致人类CF患者的肺部感染。24小时后,他们将荧光标记版本的铜绿假单胞菌引入CF患者支气管上皮细胞制成的芯片的气道通道,研究小组在CF特异性粘液中检测到的病原体数量高于健康气道芯片中的粘液。结果,促炎细胞因子水平进一步升高,从而复制了CF患者中所见的感染-炎症循环。
下一步,该团队将进一步个性化他们的CF肺气道芯片,通过生成来自同一患者的支气管上皮细胞、血管内皮细胞和免疫细胞。“在这项概念验证研究中,我们只使用了cf特异性支气管气道来自携带频繁ΔF508 CFTR突变的患者的细胞。但是不同的CFTR突变也可能影响内皮细胞和免疫细胞的功能,并且其效果不同,”共同第一作者罗伯托·普莱巴尼博士说。“通过使用来自不同突变患者的细胞开发一组患者特异性气道芯片,并直接测量芯片上不同受损CFTR离子通道的活性,可以以高度个性化的方式研究药物反应和疗效。”普莱巴尼作为意大利基耶蒂-佩斯卡拉大学的客座教授在英格伯的实验室工作,并与波特拉一起领导了英格伯小组的项目。
更多信息:罗伯托·普莱巴尼等人,在人类肺气道芯片上建模肺囊性纤维化,囊性纤维化杂志(2021)。DOI: 10.1016 / j.jcf.2021.10.004