科学家在动物模型消除关键阿尔茨海默氏症的特性
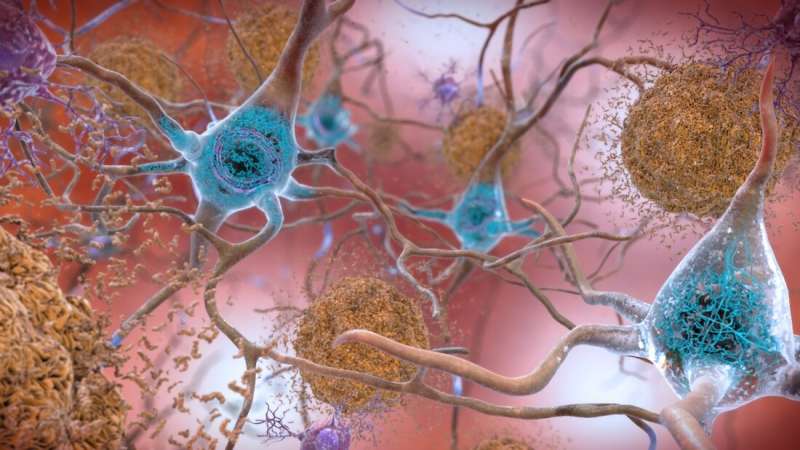
UT西南研究人员的一项研究发现,改变部分大脑细胞的生物化学废除β淀粉样蛋白斑块的形成在阿尔茨海默病小鼠模型。这一发现发表在eLife,最终可能导致治疗,防止人类的记忆状态。
“我们设想,我们抑制药物作用于相同的蛋白质在这些老鼠有一天扮演相同角色,他汀类药物在阿尔茨海默氏症心脏病,帮助阻止病情发展,“Joachim赫兹说,医学博士分子遗传学教授、神经病学和神经科学UTSW。赫兹领导了这项研究,研究生康妮黄西是一位联席作者。
将近600万美国人患有老年痴呆症,与绝大多数发展中出现迟发性的形式,65岁以后。阿尔茨海默病的特点是大脑细胞受到细胞外蛋白制成的斑块β淀粉样蛋白和细胞内缠结的异常形式的一种叫做τ的蛋白质。虽然疾病的原因并不明确,科学家们早就知道,最重要的遗传风险因素迟发性阿尔茨海默氏症是载脂蛋白E4 (ApoE4),三种变异蛋白质参与脂肪代谢的哺乳动物。ApoE4变异在人类身上,减少了阿尔茨海默氏症发病的平均年龄好几年相比有最常见的变体,ApoE3,少见ApoE2似乎对这种疾病有保护作用。
ApoE非常相似结构的三个版本,王解释道:与ApoE2相比,ApoE3包含一个氨基酸替换,导致蛋白质有更多的正电荷。ApoE4变体的包含两个氨基酸替换,导致最高正电荷三种形式的ApoE蛋白质。这些差异的机制影响晚发性阿尔茨海默氏症的风险是未知的。
在他们的新研究中,赫兹、黄和他们的同事关注早期核内体,细胞器负责分拣蛋白,回收再利用,或运输通过细胞内部细胞垃圾场称为溶酶体。以前的研究已经表明,早期核内体是扩大与ApoE4人和动物,相比之下,那些带着另外两个ApoE变体。
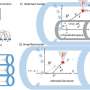
使用转基因小鼠模型阿尔茨海默病和生产ApoE4的人类形式和β淀粉样蛋白,研究人员表明,ApoE4造成这种蛋白质的正电荷聚集在早期核内体因为ApoE4的电荷匹配核内体内部的环境。这种凝结阻止这些细胞器继续他们的旅程通过细胞运输、回收,或者帮助处理其他蛋白质,包括β淀粉样蛋白。
然而,当研究人员利用基因技术关闭基因称为NHE6大脑细胞,他们发现ApoE4的负面影响被消除,并通过细胞蛋白质运输没有障碍。NHE6产生一种蛋白质,这种蛋白质作为核内体的pH值调节器,钠离子的酸性质子交换。当研究者NHE6基因关闭,消除其蛋白质从细胞,核内体早期迅速成为更多的酸性和生化变化似乎阻止淀粉样β蛋白聚合。
“抑制NHE6产生相同的保护作用ApoE2,影响我们希望最终可以复制使用药品,”黄说。
该小组计划继续研究这种机制以及如何抑制NHE6在未来的研究。
更多信息:特蕾莎Pohlkamp et al, NHE6损耗纠正ApoE4-mediated突触损伤,减少淀粉样斑块负荷,eLife(2021)。DOI: 10.7554 / eLife.72034