ATR抑制剂rp - 3500显示安全性和早期临床受益
first-in-human,第一阶段试验,德克萨斯大学MD安德森癌症中心的研究人员发现,ATR抑制剂rp - 3500是安全的和具有广阔的临床效益良好的耐受性。首席研究员蒂莫西·a·Yap博士副教授临床实验的癌症治疗,今天试验的初始数据AACR-NCI-EORTC虚拟分子靶和癌症治疗国际会议。
试验研究最大biomarker-selected测试ATR抑制剂作为一个代理在癌症窝藏合成致命的基因改变DNA损伤修复途径(DDR)。Yap和他的团队观察初步患者抗肿瘤功效先进的实体肿瘤包括卵巢癌、前列腺癌和乳腺癌癌症抗,耐火材料或偏执的标准疗法,包括乳腺癌易感基因1和BRCA2突变癌症患者曾接受了PARP抑制剂治疗。强有力的和高度选择性rp - 3500实现有意义的临床效益在多种基因改变69年34可评价的患者(49%),其中包括12名患者客观肿瘤反应,14 RECIST-defined稳定疾病患者至少16周,和八个患者早期显著降低肿瘤标记和肿瘤收缩。
“rp - 3500不仅展示了良好的和差异化的安全性,但我们的初始数据还显示有前途和不同的早期疗效,“Yap说。“虽然这个阶段我研究只有大约九个月的在有效剂量的剂量100毫克或更多的rp - 3500,我们鼓励迄今观察到在这个不易治愈的先进癌症病人的人口。”
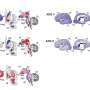
各种条件的DNA损伤,特别是在DNA双链和复制压力、DDR机制的激活一个复杂的网络。的一个关键调解人的DDR信号通路蛋白激酶ATR,它被激活在DNA复制stress-making承诺在癌症治疗的目标范围的DDR缺陷。
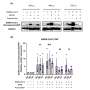
基于全基因组CRISPR-based筛选平台,17个生物标志物灵敏度rp - 3500包括ATM、BRCA1/2和其他变化识别潜在的病人选择试验。
“我们希望给每个病人的最佳机会回应只招收那些至少有其中一个突变可行的预测反应的生物标记rp - 3500,“Yap说。
研究了总共101例严重预处理先进实体肿瘤携带合成致命的基因改变,研究人员预测ATR抑制剂的敏感性。研究的主要终点是安全性和耐受性,以及推荐阶段2剂量(RP2D)和最优时间表。其他端点包括药物动力学、药效学和初步的抗肿瘤活性。
患者治疗rp - 3500的不同剂量和时间表。处理紧急的成绩最常见的不良事件包括1 - 2年级贫血、疲劳和食欲下降。三年级贫血中观察到21.8%的患者。没有4级或者更糟贫血在试验报告。
评估不良事件后,药代动力学、药效学和抗肿瘤活性,研究人员确定了RP2D rp - 3500 160毫克每日一次,3天,紧随其后的是四天。
早期的抗肿瘤活性分析显示有前途的肿瘤的临床活动类型和基因改变,包括ATM或CDK12-mutatedcastration-resistant前列腺癌,PARP inhibitor-resistant卵巢癌与乳腺癌易感基因1或RAD51C突变,BRCA1-mutated ER +乳腺癌,乳腺癌易感基因1突变的头部和颈部鳞状细胞癌和BRCA2突变黑色素瘤。
虽然这项研究正在进行,Yap鼓励的初始数据,将很快开放登记TRESR二期扩张军团。
“我们希望早期临床数据的强有力的和高度选择性ATR抑制剂提供一个明确的方向进一步发展rp - 3500,“Yap说。“我们将继续评估rp - 3500病人定义分子改变和小说也在理性的组合。”