为什么强生扔掉1500万COVID-19疫苗剂量不吓到你
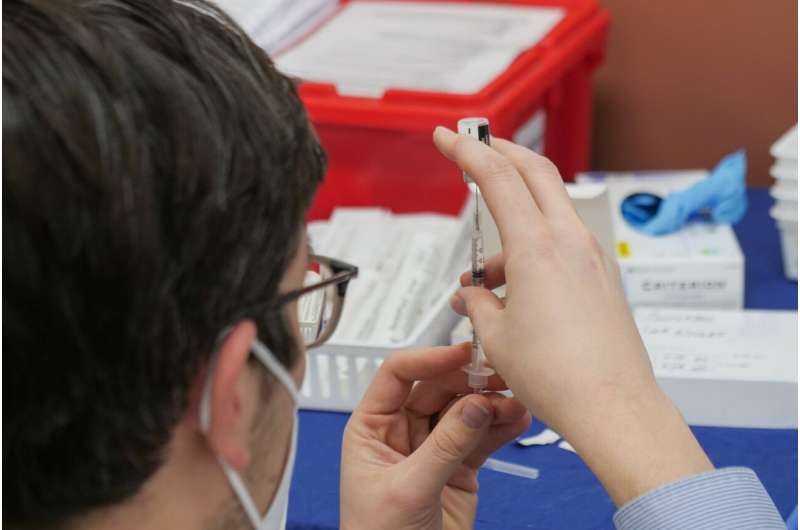
人为错误在制造厂迫使强生扔掉1500万剂其COVID-19 vaccine-enough接种7%的美国成年人口。
《纽约时报》首次报道损失3月31日,2021年,称之为“一大尴尬”疫苗制造商和分包商,紧急BioSolutions。
虽然错误的影响大小听起来令人震惊,他们也提醒人们,美国疫苗生产过程有严格的质量控制措施,旨在抓住这些问题之前达到公众。
疫苗生产是复杂的,有很多错误的潜在点。作为一个专家医疗保健业务和COVID-19疫苗推广,我密切关注疫苗生产和审批流程。质量检查的多层生产者和外部检查人员在整个过程中对保护公众健康至关重要。
检查疫苗,并再次检查他们
疫苗的开发过程是确保疫苗是安全的。
授权疫苗后,美国食品和药物管理局必须批准并定期检查每个疫苗生产设施。FDA发布的每批疫苗之前,它经历了严格的和广泛的测试,以确保疫苗的安全。在COVID-19疫苗的情况下,制造商必须提交每个质量控制测试的结果为每批疫苗48小时之前,它的分布。严格的质量控制过程导致了FDA所说的安全的疫苗供应在美国历史上。
质量控制过程也如何强生公司发现缺陷在批紧急BioSolutions设施1500万剂。
巴尔的摩的植物之一由联邦政府合同在2020年帮助有所提高产量。设备仍在等待授权美国FDA提供疫苗的使用时被发现的问题。标准的做法,强生(Johnson & Johnson)说专家的设施检查安全和质量。《华盛顿邮报》报道说,工人在2月下旬的设施弄混了阿斯利康和强生(Johnson & Johnson)疫苗的成分都产生,将整批质疑。FDA已经以前标记质量控制问题在紧急的巴尔的摩植物相关的测试潜在的治疗炭疽,据美联社获得的记录。
所有疫苗生产plants-domestic和international-require授权FDA才能供应疫苗的美国人口。目前使用的强生(Johnson & Johnson)疫苗在美国是在强生公司生产的设施在荷兰。
美国政府的操作飞行速度也参与质量控制。曾有一度,它部署16日国防部人员两个生产厂质量控制劳动力差距所以可以继续生产。
疫苗已分布后,疾病控制和预防中心继续监测病人的任何问题。
进入质量检查多少时间?
美国学年前如何关键质量控制检查和独立验证疫苗安全。1955年,小儿麻痹症疫苗的推广导致40000年诱发的脊髓灰质炎感染。
流感疫苗生产商赛诺菲说,花大约70%生产时间的质量检查,其检查疫苗的卫生官员一旦装运再次设施。
COVID-19疫苗制造商使用的新的信使rna技术现代化和辉瑞有点不具有挑战性因为它不涉及活病毒,随着传统流感疫苗。辉瑞表示,花超过一半生产时间的保证每一批的质量。
制造的改进也至关重要
制造过程改进是全面质量检测一样重要,因为错误发生。
在2020年,阿斯利康显示,制造误差导致one-and-a-half-instead两剂疫苗被给予的近3000名患者的研究。错误的研究结果,延迟个月的美国批准过程。
拜登管理要求强生加强紧急的生产过程的监督。这一事件表明,最小化的行业还有很多工作要做制造业错误。然而,我认为公众有理由仍然相信严格的质量控制过程,防止坏疫苗流通和确保疫苗安全。
进一步探索














用户评论