美国国立卫生研究院(NIH)试验检测轻、中度COVID-19的抗体和其他治疗方法
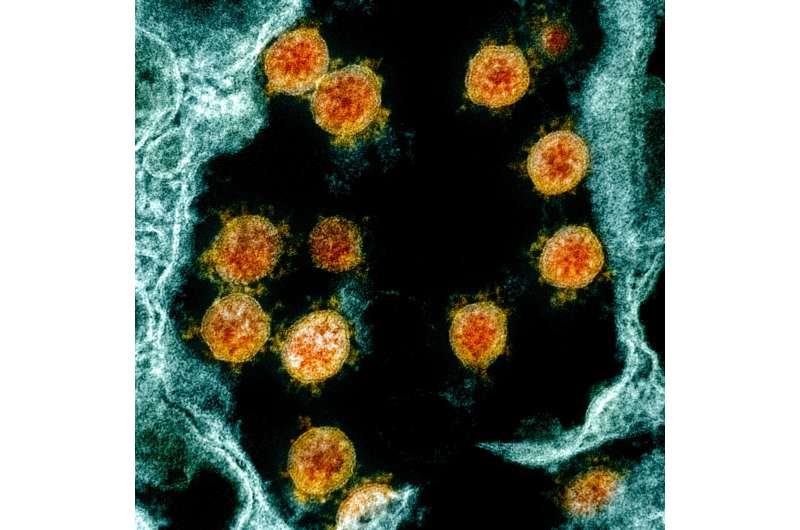
第2期临床试验将评估潜在的Covid-19潜在新治疗方法的安全性和功效,包括基于合成单克隆抗体(MAB)治疗疾病的研究治疗。由国家过敏和传染病研究所(NIAID),部分国家卫生研究院赞助的研究人员正在使用临床网站来识别目前感染SARS-COV-2的潜在患者志愿者,这是导致Covid-19的病毒,谁有轻度到中度疾病不需要住院。将被邀请参加实验治疗或安慰剂,作为一个严格设计的随机临床试验的一部分。该试验称为Activ-2,也可以在同一试用方面探讨其他实验治疗剂。
如果调查MAB显示承诺,该研究将从第2阶段扩展到第3阶段试验,以收集来自较大的志愿者的额外关键数据,毫不拖延。该审判将由NIAID-USIDED艾滋病临床试验组领导(ACTG),并将在世界各地的地点注册参与者。
Activ-2是建立的,作为NIH的一部分加速Covid-19治疗干预和疫苗(Activ),公私伙伴关系计划提起速度开发最有前途的治疗和疫苗。这项研究也接受了支持操作变形速度包括美国政府多机构研发、生产和分发抗击COVID-19医疗对策的努力。
该研究的设计是自适应的,以实现最短时间框架中的最大灵活性。如果是实验治疗在第一阶段似乎有效,可以在更大的志愿者组中迅速前进。该研究还可以适用于测试额外的治疗方法。
“我们已经从其他适应性治疗中看到了令人鼓舞的快速结果试用美国国家卫生研究院院长弗朗西斯·s·柯林斯博士说。“在ACTIV下,特定的治疗方法将根据其成功的可能性进行优先排序。ACTIV下的优先治疗方案将使用强调灵活性的主方案,使这些关键试验能够在治疗显示出希望时进行,而不会导致延迟。”
该试验中测试的第一种治疗药物将是LY-CoV555,这是礼来公司(Eli Lilly and Company,印第安纳州印第安纳波利斯)生产的一种研究性单克隆抗体。Lilly - cov555是Lilly与AbCellera Biologics(不列颠哥伦比亚省温哥华市)合作的产物。抗体是免疫细胞产生的抗感染蛋白质。所谓的中和抗体针对特定的病毒或其他病原体。这种抗体是AbCellera与NIAID的疫苗研究中心合作发现的,是从一种血液样本从回收的Covid-19患者。然后在实验室中合成该抗体的拷贝 - 术语“单克隆”是指这些实验室制造的抗体。
"Using an antibody generated by the immune system of a recovered COVID-19 patient gives us a jump start on finding a safe and effective therapeutic," said NIAID Director Anthony S. Fauci, M.D. "Investigating a variety of different therapeutics, including monoclonal antibodies, will help ensure that we advance towards an有效待遇对于尽可能快地患有Covid-19病的人们。“
审判的初始阶段旨在注册大约220名志愿者,他最近经历了Covid-19的症状,并对病毒进行了测试阳性,但不会住院。一旦注册,它们将随机分配到两组中的一组:110志愿者将接受Ly-Cov555的静脉注射(IV)输注,110名志愿者将获得盐水溶液的安慰剂输注。输液需要大约一个小时才能提供,然后之后将观察到志愿者来注意任何反应。
在接下来的28天内,参与者将参加一系列临床医生的诊所或家庭访问,以跟踪他们的Covid-19症状。调查人员还将检查来自SARS-COV-2的RNA,仍然可以使用标准的鼻咽拭子在参与者的鼻子和唾液中检测到。由于Covid-19的人往往具有异常低的血氧水平,所以参与者将接受脉搏血氧试验,以帮助确定研究治疗是否对血氧水平具有积极影响。他们还将提供血液样本,以帮助研究人员了解实验治疗方法如何在其身体上运作,以及它们是否影响了他们的SARS-COV-2感染过程。参与者将收到额外的后续行动最多24周。
第2阶段试验的主要目标是评估安全性,看看调查治疗是否可以通过研究第28天降低症状的持续时间,并看看调查治疗是否可以增加鼻咽拭子中未检测到的参与者的比例具体时间点。如果没有严重的安全问题,并且如果调查治疗似乎符合其他具体的其他标准(例如充分降低症状的持续时间或志愿者身体中的病毒载量),则试验将转变为第3阶段并注册1,780个额外的门诊志愿者,共有2,000名试验参与者。第3阶段研究的主要目标是确定调查治疗是否可以通过研究第28天预防入院或死亡,同时还继续评估其安全性。第3阶段的参与者将不提供鼻咽拭子,尽管它们仍将进行自集的前鼻拭子,并且他们将参加较少的诊所访问。
The study team is led by Protocol Chair Davey Smith, M.D., of the University of California, San Diego, David Wohl, M.D., of the University of North Carolina at Chapel Hill (UNC), and Kara W. Chew, M.D., and Eric S. Daar, M.D., both of the University of California, Los Angeles (UCLA),serve as protocol vice-chairs. The ACTG network is led by chair Judith Currier, M.D. (UCLA) and co-chair Joseph Eron, M.D. (UNC).
为确保以安全有效的方式进行试验,独立数据和安全监测委员会将监督审判并定期审查累积数据。
进一步探索










用户评论