信用:CC0公共领域
由于其内在性质和外部环境,中枢神经系统(CNS)的再生能力主要受限。传统思维认为,一旦大脑受伤,就无法修复和恢复组织正常。然而,这一概念由最近的一项研究受到挑战。
微胶质细胞很长髓细胞在中枢神经系统(CNS)Elmore和Green等报道了新发现的小胶质祖细胞细胞在神经元2014年。该发现显示了成人大脑中的第一次小胶质化祖细胞,为此提供了潜在的见解再生医学.然而,重新灌注的微胶质细胞的起源仍然热烈讨论,重新灌注的小胶质细胞来源仍然存在争议。
最近,题为“重新灌注的微胶质细胞的研究文件”公布了题为“重新灌注的微胶质细胞源自急性微胶质细胞增殖”自然神经科学中国科学院深圳先进技术研究院(SIAT)的博鹏实验室的研究。在这篇论文中,彭教授和他的同事们通过一系列命运图谱的方法,成功地破解了大脑中小胶质细胞再生的起源。
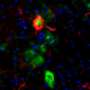
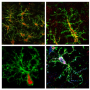
研究人员首先通过曲静脉排除了重新灌注的微胶质细胞的血液来源,一种手术方法,用交换血细胞产生嵌合小鼠(图1A)。然后,它们证明重新灌注的小胶质细胞没有与巢蛋白阳性祖细胞(图1B)分化。
他们还证明了星形胶质细胞,oligodendrocyte前体细胞(OPCS)和神经元不是重新灌注的微胶质细胞的前体细胞(图1c)。相比之下,大脑中的所有重新灌注的小胶质细胞源自药理消融(<1%)后少数小胶质细胞的增殖,以及瞬时表达巢蛋白(图1D)。
这一结果为小胶质细胞的再生提供了坚实的证据,表明小胶质细胞的再生仅仅来源于残留的小胶质细胞,而不是新生的祖细胞,表明成人大脑中没有小胶质细胞的祖细胞。此外,通过RNA测序,研究人员发现,重建的小胶质细胞可能与稳态和病变大脑中的驻留小胶质细胞具有相似的功能。
此外,视网膜是中枢神经系统的重要组成部分。成年哺乳动物视网膜的细胞再生能力甚至比大脑还要有限。虽然在视网膜中有少量细胞零星地再生,但之前没有观察到大量的细胞再生。
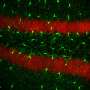
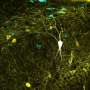
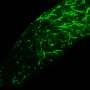
在题为“视网膜微胶束repopulation模型的微凝血血管血管胶质细胞的双重视网膜起源”的纸上,彭及其同事发现CSF1R的抑制消除了视网膜(100%)的所有常驻小胶质细胞(图2),与99%的大脑相比。
如果视网膜上的小胶质细胞再生机制与大脑(图1),新生的小胶质细胞不会出现并重新填充视网膜,因为耗尽后没有存活的小胶质细胞(图2)。作者发现,在消除CSF1R抑制后,新的小胶质细胞出现并迅速重新填充整个视网膜(图2)。这是首次在成年哺乳动物视网膜中观察到强大而大规模的细胞再生。视网膜小胶质细胞的起源是一个谜。
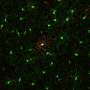
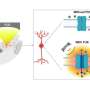
然后提交人调查了重新掺杂的视网膜小胶质细胞的起源,发现重新灌注的视网膜微胶质细胞有两种不同的起源群体:大多数是中心出现的小胶质细胞;和少数群体,其是外围的微胶质细胞。中心出现的小胶质细胞被源自视神经中的残余小胶质细胞,而外围新兴的小胶质细胞衍生自睫状体/虹膜中的巨噬细胞(图3)。
通过小胶质细胞再生模型,作者首次在成年哺乳动物视网膜中观察到强大和大量的细胞再生。此外,他们首次发现了成人视网膜中小胶质细胞的视网膜外起源,为小胶质细胞的起源和维持提供了新的线索小神经胶质细胞在视网膜中。
这些研究主要由Bo Peng的实验室与香港大学延夏饶博士合作,上海交通大学省泰飞元教授合作。Yubin Huang博士和Zhen Xu博士是这两项研究的联合第一作者。
更多信息:黄玉斌等,再生小胶质细胞仅来源于急性衰竭后残留小胶质细胞的增殖,自然神经科学(2018)。DOI:10.1038 / S41593-018-0090-8
所提供的中国科学院