研究人员开发了一种远程控制癌症免疫治疗系统
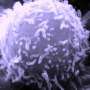
一组研究人员开发了一种基于超声波的系统,可以非侵入性地远程控制活免疫T细胞的遗传过程,使它们识别并杀死癌细胞。
非侵入性和远程操作是非常必要的细胞研究人员说,尤其是在动物和人类的转化应用方面。
该团队开发了一种创新的方法来使用机械遗传学(一种专注于物理力和细胞和组织机械特性的变化如何影响基因表达的科学领域)来远程控制基因和细胞激活。研究人员使用超声波机械干扰T细胞,然后将机械信号转化为细胞的遗传控制。
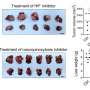
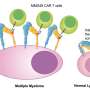
在这项研究中,研究人员展示了他们的远程控制机械遗传学系统如何用于设计嵌合抗原受体(CAR)表达的T细胞,可以靶向和杀伤癌症细胞.工程CAR-T细胞具有机械传感器和遗传转导模块,可以通过微泡放大超声远程激活。
加州大学圣地亚哥分校生物工程教授王英晓(Peter Yingxiao Wang)说:“CAR-T细胞疗法正在成为一种改变癌症治疗范式的治疗方法。”“然而,在基于car的免疫疗法被广泛采用之前,仍然存在重大挑战。例如,CAR-T细胞针对非恶性组织的非特异性靶向可能危及生命。这项工作最终可能导致CAR-T细胞免疫治疗实体肿瘤的前所未有的精确性和效率,同时最大限度地减少肿瘤外毒性。”
该团队汇集了王教授和钱舒教授的实验室,他们都是雅各布斯工程学院和加州大学圣地亚哥分校医学工程研究所的生物工程教授,与南加州大学的Kirk Shung教授和纽约纪念斯隆凯特琳癌症中心的Michel Sadelain教授合作。研究人员将他们的研究结果发表在了1月15日的《科学》杂志上美国国家科学院院刊加州大学圣地亚哥分校(UC San Diego)博士候选人潘怡嘉(Yijia Pan)是第一作者。
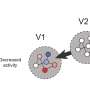
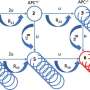
研究人员发现,与链霉亲和素结合的微泡可以耦合到细胞表面,在细胞表面表达机械敏性Piezo1离子通道。当暴露在超声波下时,微气泡振动并机械地刺激Piezo1离子通道,让钙离子进入细胞。这会触发下游通路,包括钙调神经磷酸酶激活、NFAT脱磷酸化和转位到细胞核。核易位的NFAT可以结合到基因转导模块的上游反应元件,启动嵌合抗原受体(CAR)的基因表达,以识别和杀死目标癌细胞。