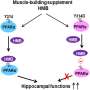
第二阶段3 LMTX发表了研究结果
TauRx疗法有限公司今天公布完整的LMTX第二三期临床研究的结果,第一个τ聚合抑制剂在阿尔茨海默病,在线发表阿尔茨海默氏症期刊》上。
从这个研究结果(硫氧还蛋白- 237 - 005)是一致的与第一阶段3研究最近发表在《柳叶刀》[(硫氧还蛋白- 237 - 015)Gauthier et al . 20161]在轻度至中度阿尔茨海默氏症,在支持的假设LMTX可能有效单药治疗在剂量低至4毫克每日两次。
最新研究(硫氧还蛋白- 237 - 005)的疗效和安全性研究800年LMTX轻度阿尔茨海默氏症患者的剂量100毫克或4毫克(为了控制剂量)在18个月的治疗期,每天两次。
早期的研究结果显示显著差异的两个更高的剂量LMTX(75毫克和125毫克每日两次)当作为单一疗法与预期相比4毫克剂量控制作为单一疗法或附加疗法目前在指定批准治疗阿尔茨海默病的事后分析。进一步分析,同样支持单一疗法与附加治疗相比差异被发现在病人服用4毫克剂量的两倍。
因此,数据库锁定和截断符号之前,硫氧还蛋白- 237 - 005的主要分析被修改比较100毫克每天两次LMTX单目标控制、和4毫克每日两次作为单药治疗相比,相同的剂量作为添加治疗non-randomised群分析。目的是测试第一项研究的结果是否可以被确认为主要在第二个独立研究结果具有较强的控制对统计误差。
第二项研究的结果显示,支持相同的显著差异LMTX单方要求统计阈值的在两个比较p < 0.025 co-primary临床疗效端点的认知(ADAS-cog)和功能(ADCS-ADL)的结果。
LMTX单一疗法和附加治疗组,全脑萎缩(通过核磁共振扫描测量)最初进展作为轻度阿尔茨海默氏症患者的预期。然而,9个月的治疗后,整个在单药治疗脑萎缩患者的年增长率降低显著,成为典型的报道在正常老年人控制没有阿尔茨海默氏症。的可比的附加治疗组进展报告轻度阿尔茨海默氏症患者。
同样,更多的从正子扫描发现硫氧还蛋白- 237 - 005表明颞叶葡萄糖吸收的下降在那些接受LMTX单药治疗的患者明显小于通常报告轻度阿尔茨海默氏症患者。
当各种分析纠正潜在的严重性或诊断基线差异单一疗法和附加疗法组,结果依然强劲意义重大。
“虽然单一治疗组在第一和第二阶段3 LMTX研究仍小——分别为15%和20%的确认同样的模式在第二独立研究的结果意味着他们不太可能有机会发现,“克劳德Wischik教授说,阿伯丁大学和执行主席TauRx疗法。
“总体保持利率在第二项研究中单一疗法和附加治疗组相似,所以微分的提现率不能解释。同样,看到相同的结果在第二只研究在北美、西欧和澳大利亚意味着第一项研究并不是典型的以某种方式通过其包含的非西方国家。找到相同的模式结果在临床和影像学的结果也意味着它们不能被解释为安慰剂效应在患者进入治疗第一次。”
Wischik教授继续评论:“虽然这些结果来自non-randomised群体分析,很多东西指向真实的治疗影响而不只是病人采取或不采取差异的标准治疗。分析显示,脑萎缩速度放缓是一个前后分析单一疗法的患者自己的控制,因此不依赖于附加治疗患者比较。我们也开始理解LMTX之间的负作用的药理学基础和标准治疗,因为我们已经看到同样的事情发生在动物模型的tau蛋白质聚合。”
“这些非常重要的结果支持进一步的验证tau-based治疗阿尔茨海默氏症,”乔治·佩里说院长科学、德克萨斯大学圣安东尼奥和主编的《阿尔茨海默氏症。
该研究的第一作者,戈登-威尔科克,衰老学名誉教授和名誉临床高级研究员纳菲尔德系牛津大学临床神经科学评论道:“这些数据表明需要进一步的随机对照试验来评估疗效的患者没有服用低剂量LMTX当前治疗。”
进一步的随机对照研究LMTX不久将开始的4毫克剂量将与安慰剂比较的两倍病人与阿尔茨海默氏症疾病不接受其他批准治疗这种情况(胆碱酯酶抑制剂和/或美金刚胺)。
更多信息:戈登·k -威尔科克等。低剂量的潜力Leuco-Methylthioninium Bis (Hydromethanesulphonate) (LMTM)单药治疗轻度阿尔茨海默氏症的治疗:队列分析修改主要结果在三期临床试验,阿尔茨海默氏症期刊》上(2017)。DOI: 10.3233 / jad - 170560