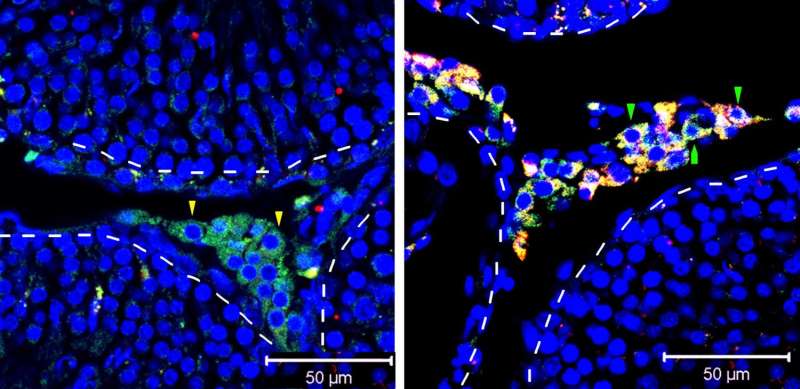
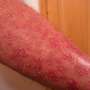
如图所示,移植后表达gfp的成纤维细胞(黄色箭头,左)和诱导的leydigg样细胞(绿色箭头,右)迁移到精小管的间质区域(“白色支架”所示)。诱导的间质样细胞表达类固醇生成的所有必需酶,并合成黄体生成素触发的睾酮。信贷:下苏
男性性腺功能减退症是一种导致大约30%的老年男性睾丸激素水平下降的疾病,但目前可用的治疗方法可能产生严重的副作用。在12月22日发表的一项研究中干细胞的报道在美国,研究人员开发了另一种方法,将成人皮肤细胞直接转化为有功能的睾丸激素产生细胞。当移植到性腺功能减退的雄性啮齿动物体内时,这些所谓的leydig样细胞存活下来,并恢复了正常的睾丸激素水平。
“我们的研究是第一个报告生成Leydig的方法细胞通过直接的细胞重编程,”该研究的高级合著者、暨南大学黄亚东说。“这种间质细胞的替代来源将对基础研究具有重要意义,并提供了诱人的临床应用前景。再生医学。"
男性性腺功能减退的症状包括情绪紊乱、性功能障碍、肌肉质量和力量下降以及骨密度下降。一个主要原因是睾丸中产生睾丸激素的间质细胞功能障碍。睾酮替代疗法可以缓解间质细胞衰竭引起的一些症状,但也可能增加前列腺和心血管并发症的风险,如血栓的形成。
间质细胞移植是一种很有前途的替代激素替代疗法,提供激素的生理模式较长一段时间。然而,基于干细胞的方法是昂贵的,耗时的,并受到伦理问题和肿瘤形成风险的限制。黄和暨南大学的共同高级研究员苏志坚认为,将成人皮肤细胞直接转化为间质细胞将是一种更快、更安全的再生医学方法。
为了验证这一想法,研究人员筛选了11个可能影响间质细胞产生睾丸激素能力的转录因子。他们利用慢病毒载体强迫三个转录因子Dmrt1、Gata4和Nr5a1的表达,能够直接将小鼠皮肤细胞重新编码为功能性的leydig样细胞,这些细胞显示出正常的基因活性,并能够产生睾丸激素。当移植到性腺功能减退的大鼠或小鼠睾丸后,这些细胞存活并恢复正常睾酮水平。
根据作者的说法,未来的研究应该致力于提高该方法的效率,以产生接近成年间质细胞的纯细胞群。就他们自己而言,研究人员正在更详细地研究这种直接转换背后的机制皮肤细胞成Leydig-like细胞。为了使研究结果与患者更相关,他们也在研究使用小分子和其他非病毒方法的直接细胞转化策略。“最后,我们希望这项研究将为临床试验铺平道路,试验一种新的再生医学方法来治疗男性雄激素缺乏,”苏说。
更多信息:干细胞的报道, Yang等人:“通过定义的因子对小鼠成纤维细胞向类间质细胞直接重编程”www.cell.com/stem-cell-reports…2213 - 6711 (16)30272 - 7,DOI: 10.1016 / j.stemcr.2016.11.010
期刊信息:干细胞的报道
所提供的细胞出版社