研究强调基因可能导致治疗肌萎缩性侧索硬化症
内盖夫本-古里安大学(BGU)的研究人员发表了一项新的研究,描述了一种新的分子机制,可能导致肌萎缩性侧索硬化症(ALS)新疗法的开发。这项研究发表在著名的PNAS(美国国家科学院院刊).
肌萎缩性侧索硬化症,也被称为卢伽雷氏病,是一种致命神经退行性疾病这会导致控制随意肌的运动神经元死亡。由于肌肉萎缩导致的渐进性虚弱和瘫痪导致说话、吞咽和最终呼吸困难。这种疾病通常在40岁至60岁之间发病,从发病到死亡的平均生存期为2至5年。
在大约90%的病例中,病因尚不清楚,但大约10%是遗传的。大约20%的这些遗传病例是由SOD1基因(超氧化物歧化酶)的突变引起的,这导致了“错误折叠”SOD1蛋白的积累,引发了选择性杀伤运动神经元.
“正确的蛋白质折叠是至关重要的,这就是为什么我们专注于各种复杂的细胞机制,包括分子伴侣,促进有效折叠和防止毒性,”阿德里安·以色列森博士说,他是BGU生理学和细胞生物学系细胞和分子神经退行性变实验室的负责人。
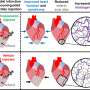
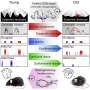
本研究首次报道了“内源性多功能蛋白巨噬细胞迁移抑制因子(内源性多功能蛋白巨噬细胞迁移抑制因子,MIF)”,一种调节细胞炎症和免疫的基因,作为一种错误折叠的SOD1的伴侣小鼠模型.研究人员证明,在家族性ALS突变SOD1小鼠模型中完全消除MIF会增加错误折叠的SOD1积累。这也加速了疾病的发病和疾病的晚期进展,并缩短了表达突变SOD1的小鼠的寿命。
“这项研究通过调节MIF水平,为MIF在抑制ALS中错误折叠SOD1选择性积累方面的潜在治疗作用提供了见解,”以色列森博士说。
以色列森博士的实验室专注于导致神经退行性疾病(如阿尔茨海默病、帕金森病和亨廷顿病)发病和发展的细胞和分子机制,特别强调渐冻症。
更多信息:Marcel F. Leyton-Jaimes等人。内源性巨噬细胞迁移抑制因子降低了ALS小鼠模型中错误折叠SOD1的积累和毒性美国国家科学院院刊(2016)。DOI: 10.1073 / pnas.1604600113