Kruppel-like通过早期生长反应因子12促进大肠癌蛋白质1
临床前研究的结果通过音乐调查在2016年7月的报告《公共科学图书馆•综合》首次展示,转录因子KLF12促进CRC细胞生长,在某种程度上,通过激活EGR1。此外,数据表明,KLF12和EGR1水平表现为协同作用与可怜的CRC预测。
CRC是第三个最常见和第三致命癌症在美国。像大多数癌症一样,CRC发展是受一系列改变的遗传变异和表观遗传变异基因表达。反过来,这改变了基因表达启动肿瘤和支持他们的发展。因此,转录因子调节基因表达和信号通路在致癌作用长期以来一直研究作为潜在的治疗靶点。
博士雷蒙德•杜布瓦音乐医学院的院长,生物化学和分子生物学教授和高级作者这篇文章集中在理解炎症在癌症的作用。“我们已经在我的实验室研究炎症和癌症之间的联系有一段时间了,已经确定,一些炎症介质刺激癌症的进展,”杜波依斯说。“我们发现KLF12急剧增加在某些癌症炎症的存在,所以我们正试图确定的具体分子机制负责这些影响。”
其他研究人员正在研究肾脏发展之前确定转录因子KLF12 AP-2α基因的转录抑制因子。当时发现AP-2α表达式也减少了在先进的CRC肿瘤组织与正常组织相比,AP-2α提升CRC入侵的损失。这个连接照亮一个潜在的KLF12和CRC之间的联系。体外研究表明,KLF12促进胃癌(GC)细胞增殖和入侵,这KLF12水平升高约40%的低分化GCs和与肿瘤大小有关。此外,最近的全基因组分析发现高KLF12水平在大约40%的食管腺癌和唾液肿瘤的45%。直到现在,然而,在CRC KLF12的作用仍不清楚。
音乐研究团队设计一系列的体外和体内实验来阐明KLF12在CRC的角色。第一组研究检查KLF12表达在人类CRC 7细胞株。他们发现,KLF12不仅在6 7细胞系的表达,而且其表达导致细胞数量和增加KLF12击倒导致细胞数量减少。此外,他们还发现表达KLF12导致的形成更大的盲肠的肿瘤而KLF12击倒导致形成较小的盲肠的肿瘤,而控制。因此,这组实验表明KLF12促进CRC生长提高癌症细胞增殖和/或生存。
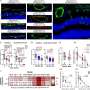
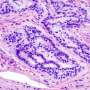
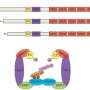
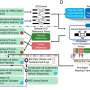
下一组实验关注的是澄清这KLF12目标基因可能参与调节CRC的增长。使用微阵列分析,研究人员发现,KLF12表达多个基因改变包括EGR1。之前报道,KLF12调节某些目标基因的表达通过绑定到CACCC主题。他们发现EGR1启动子可能包含两个KLF12 dna结合图案位于-1488个基点(主题1)和-808个基点(主题2)相对于转录起始站点。使用芯片分析,音乐研究小组发现KLF12,的确,强烈地绑定到EGR1子主题2而不是主题1。体外实验表明,信使rna和蛋白质含量,CRC细胞水平检测不到的KLF12 EGR1最低水平的表达与细胞表达高水平的KLF12相比。体内研究使用过度的小鼠肿瘤细胞植入CRC KLF12表明EGR1表达上调相比,小鼠植入细胞的控制。此外,产生的人类CRC组织标本染色相同的模式。总的来说,这些结果表明,KLF12直接激活EGR1 CRC。
第三组实验看是否EGR1介导KLF12对肿瘤细胞生长的影响。结果表明,EGR1击倒KLF12-induced减少肿瘤细胞生长,而EGR1过表达促进了CRC体外细胞生长以及肿瘤生长在老鼠模型中。这组研究的结果,因此,表明KLF12增强CRC细胞生长通过激活EGR1。
最后一组的实验评估KLF12和EGR1水平是否与CRC患者的预后。使用从公开的微阵列基因表达数据数据库(莫菲特(n = 177);范德堡大学医学中心(n = 55)), CRC患者分层KLF12和/或EGR1表达式。这些数据表明,高水平的患者KLF12或EGR1相比有更糟糕的结果与低水平的这些基因,和那些高水平的KLF12和EGR1存活率最低。
这是第一个研究澄清KLF12 CRC肿瘤的生长和发展的作用似乎发生,至少在某种程度上,通过EGR1激活。KLF12发现协同贡献和CRC患者EGR1产生最坏的结果照亮他们的潜能开发新的治疗方法。需要更多的研究来进一步阐明KLF12 CRC进展和其潜在的作用作为一种新颖的预后标志物和治疗的目标。