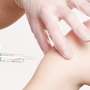
一个人在2020年12月21日星期一的荷兰进入阿姆斯特丹的欧洲药物局,EMA的人类药物委员会持有一个特殊的,完全虚拟的会议,以得出评估辉瑞-Biontech Covid-19疫苗的评估。(美联社照片/彼得·德琼)
周一,欧盟(eu)正式批准生物科技(BioNTech)和辉瑞(Pfizer)研发的冠状病毒疫苗在欧盟27个成员国中使用,这让各国有望在圣诞节后不久开始为本国公民注射首批疫苗。
欧盟的执行委员会在欧洲药物局表示疫苗符合安全质量和质量标准之后几个小时给了绿灯。预计布鲁塞尔将需要两三天,以支持市场授权举措。
欧盟委员会主席乌苏拉·冯·德莱恩说:“正如我们承诺的那样,这种疫苗将在相同条件下同时提供给所有欧盟国家。”“这是结束这艰难的一年,并最终开始翻开新冠肺炎新篇章的一个非常好的方式。”
她说,疫苗的运送将于本周六开始,接种工作将于12月27日至29日在欧盟各地开始。
该疫苗几周前在英国和美国获得批准,这促使欧盟各国政府向EMA施压,要求其加快批准程序,因为整个欧洲大陆的病毒病例再次激增。
EMA最初将12月29日为评估疫苗的日期,但是在德国政府和其他机构呼叫后呼吁将会议转移到周一,以便该机构更快地移动。
2020年12月21日,德国美因茨,生物技术公司BioNTech的德国总部在镜子里。预计欧洲医疗机构EMA将在周一允许生物技术公司的疫苗进入欧盟。(美联社照片/ Probst迈克尔)
EMA的专家委员会负责人Harald Enzmann驳回了任何建议,即政治影响受到决定。
他告诉记者:“焦点完全集中在科学上。”“这是一个科学评估,句号。”
总部位于阿姆斯特丹的EMA负责批准欧盟27个成员国、冰岛、列支敦士登和挪威的所有新药和疫苗。它大致相当于美国食品和药物管理局。
该疫苗已经在至少15个国家获得了某种形式的监管授权。
英国,加拿大和美国授权根据紧急条款使用疫苗,这意味着镜头是一个未经许可的产品,其临时使用是由约翰·霍普金斯大学造成近170万人造成的大流行。
一辆卡车在12月21日星期一的比利时进入普瑞斯的辉瑞制造厂。欧洲药物局周一会议,考虑批准由Biontech和PFizer开发的冠状病毒疫苗,这将是第一个被授权用于使用的冠状病毒疫苗欧洲联盟。在这次闭门会议举行几周前,英国和美国的监管机构根据紧急条款批准了枪击事件。(美联社照片/ Valentin Bianchi)
星期六,瑞士成为第一个按照正常许可程序批准该疫苗的国家。EMA的有条件上市许可也遵循了常规程序,只是在加速进度和制药公司提交下一年疫苗的后续数据的条件下。
虽然许多人对疫苗的授权感到敏感,但在欧洲和其他地方也有担忧,关于开发出镜头的速度。通常,疫苗需要多年的时间来发展和批准,而不是几个月。
该机构在上周的一份声明中强调,只有在科学评估表明疫苗的总体益处大于风险后,该疫苗才会获得批准。
科学家们仍在等待更多长期的随访数据,以了解疫苗的免疫能持续多久,以及是否有任何罕见或严重的副作用。疫苗的最终测试仍在进行中,还需要更多关于疫苗是否对儿童有效的信息。EMA的专家还说,关于孕妇的数据是有限的,医生应该根据具体情况做出决定。
2020年12月21日,周一,比利时普乌尔,辉瑞制造公司办公室的窗户上挂着这样的标语。欧洲药品管理局(European Medicines Agency)周一开会,考虑批准一种由BioNTech和辉瑞(Pfizer)研发的冠状病毒疫苗,这将是首个获准在欧盟使用的疫苗。在这次闭门会议举行几周前,英国和美国的监管机构根据紧急条款批准了枪击事件。(美联社照片/ Valentin Bianchi)
疫苗不是用冠状病毒本身制成的,这意味着任何人都不可能因为注射而感染。相反,这种疫苗含有一段遗传密码,可以训练免疫系统识别病毒表面的带刺蛋白。
在英国开始接种疫苗的当天,当局警告严重过敏的人不要接种疫苗,因为有两人出现了严重的过敏反应;目前还不清楚这些反应是否由疫苗引起。
The U.S. Centers for Disease Control and Prevention said that as of Friday there had been six cases of severe allergic reaction in the U.S. out of more than a quarter-million shots of the BioNTech-Pfizer vaccine given, including in one person with a history of vaccination reactions.
对一种新发现的似乎更容易传播的菌株的担忧,使已经可怕的死亡人数雪上加霜。但是专家们对新疫苗仍然有效表示有信心。
2020年12月21日,欧洲药品管理局(EMA)人类药物委员会在荷兰阿姆斯特丹举行了一次特殊的、完全虚拟的会议,以结束对辉瑞-生物科技COVID-19疫苗的评估。(美联社照片/彼得·德琼)
药物监管机构负责人埃默尔·库克(Emer Cooke)在一次闭门会议后表示,“目前我们可以说,没有证据表明该疫苗不会对冠状病毒的新变种起作用。”在这次会议上,专家们一致建议16岁以上的人群接种该疫苗。
但她补充说,一段时间可能需要戴着面具,洗手和社会偏差等保护措施。
库克说:“疫苗本身并不是让我们恢复正常生活的灵丹妙药。”“但首支疫苗的批准绝对是朝着正确方向迈出的重要一步,表明2021年可能比2020年更光明。”
欧盟已经订购了3亿剂辉瑞生物科技的疫苗;每个人需要注射两针,这意味着欧盟近4.5亿居民需要接种其他疫苗。
2020年12月21日,周一,比利时普乌斯的辉瑞制造公司,卡车停在装载区。欧洲药品管理局(European Medicines Agency)周一开会,考虑批准一种由BioNTech和辉瑞(Pfizer)研发的冠状病毒疫苗,这将是首个获准在欧盟使用的疫苗。在这次闭门会议举行几周前,英国和美国的监管机构根据紧急条款批准了枪击事件。(美联社照片/ Valentin Bianchi)
EMA计划在1月6日召开会议,决定Moderna生产的另一种疫苗是否应该获得许可。牛津大学(Oxford University)、阿斯利康(AstraZeneca)和杨森(Janssen)研发的一种疫苗正在接受审查,但这两家公司都没有向EMA提出正式申请,以批准他们的疫苗。
“对我们生物科技来说,今天是个特别个人、特别感人的日子,”这家德国公司的首席执行官兼联合创始人乌格·沙欣(Ugur Sahin)说。“作为欧盟的中心,我们很高兴能够向可能提供欧洲首个疫苗的目标迈进一步,以帮助抗击这种毁灭性的流行病。”
©2020美联社。保留所有权利。未经允许,不得出版、广播、改写或转载。