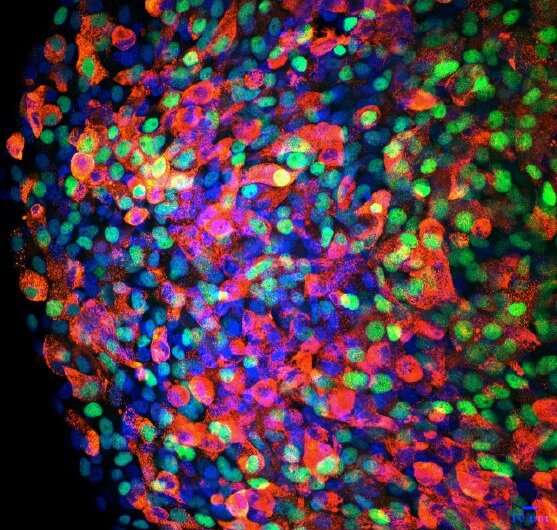
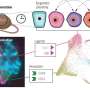
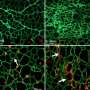
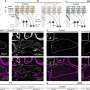
共焦显微照片人多能干细胞分化beta-like免疫荧光染色的细胞在3 d瀑样文化与一个anti-C-peptide抗体(红色)和一个anti-PDX1抗体(绿色)。DAPI染色细胞核。信贷:海特马/怀特黑德研究所
1型糖尿病是一种自身免疫性疾病,发生在t细胞的免疫系统攻击人体自身的胰岛素生产细胞,称为β细胞,在胰腺中。通常在儿童和年轻成人诊断,1型糖尿病占所有糖尿病病例的百分之五左右。
1型糖尿病的潜在生物学研究的原因是一个棘手的问题。首先,一个人开始的时候显示症状,T -细胞已经被破坏β细胞长period-months甚至数年。同时,最初的触发疾病往往是不清楚;大量的β细胞蛋白质可以出发免疫反应。
在9月22日发表的一项研究细胞医学报告怀特黑德研究所的研究人员在实验室中,创始成员鲁道夫Jaenisch展示一个新的实验系统更准确地研究1型糖尿病的机制,关注一个人的β细胞如何应对从自己的免疫系统的攻击。在这一过程中,他们揭示疾病的特性,可以为未来的治疗目标。
“我们的问题是,假设T细胞被激活;从的角度β细胞接下来会发生什么?我们能找到一些潜在的干预机会?”海特马,Jaenisch的实验室的博士后,这项研究的第一作者。
妈,Jaenisch,麻省理工学院的生物学教授,雅各Jeppesen,诺和诺德公司的糖尿病和代谢生物学、合成生物学的方法来实现这一目标。
研究人员研制出一种通过诱导系统人类多能干细胞分化成功能性胰腺β细胞,并添加一个名为CD19抗原模型使用CRISPR这些细胞的技术。他们建立了这些细胞,是产生胰岛素的β细胞植入糖尿病小鼠;在接收细胞,老鼠经验丰富的葡萄糖水平的改善。
然后复制自身免疫性疾病的组件使用工程称为CAR-T细胞的免疫细胞。CAR-T细胞是特制的t细胞攻击某种类型的细胞;例如,他们可以针对肿瘤细胞治疗某些类型的癌症。对于糖尿病模型,研究人员设计抗原CD19细胞含有受体模型。
当研究者cocultured合成β细胞和CAR-T细胞,他们发现系统运行良好模拟1型糖尿病的一个简化版本:CAR-T细胞攻击β细胞,使它们进入细胞死亡的过程。研究人员也能够实现人性化的小鼠的策略。
使用他们的新实验系统,研究人员能够识别一些有趣的因素参与糖尿病的β细胞的反应条件。首先,他们发现,β细胞提高了生产的蛋白质PDL1等保护机制。PDL1是无细胞的蛋白质在体内,在正常情况下,阻止免疫系统攻击他们。
PDL1水平变化已经在先前的研究与1型糖尿病有关。现在,妈妈想知道可以拯救β细胞的免疫攻击的诱导表达的更有用的蛋白质。“我们发现,我们可以帮助β细胞PDL1给他们更高的表达,”他说。“当我们这样做,他们可以做得更好的模式。”If validated in human cells, increasing expression of PDL1 could be evaluated as a potential therapeutic method, Ma said.
另一个发现有关细胞t细胞攻击后死亡的方式。马发现被调节的基因相关的β细胞被攻击而不是通常的形式的细胞死亡,细胞凋亡,但更多的炎症性和暴力的叫做pyroptosis细胞死亡。
pyroptosis“有趣的地方是,它会导致细胞释放其内容,“马说。“这是与细胞凋亡,这被认为是自身免疫反应的主要机制。我们认为pyroptosis可能在推动这种自身免疫反应中发挥作用,因为β细胞的内容包括多个潜在的抗原。如果这些被释放,他们可以挑选出抗原呈递细胞,开始启动自身免疫。”
pyroptosis的过程中β细胞自身免疫可能与β细胞ER应激有关,一个高度分泌细胞类型。事实上,一个ER应激诱导化学增加pyroptosis的标志。
如果研究人员能找到一种方法来抑制pyroptosis牢牢掌握在人类的过程中,它可能会降低自身免疫反应的严重程度是1型糖尿病的标志。Pyroptosis是由一种叫做caspase-4的蛋白质,在实验室里可以抑制。“如果可以验证患者β细胞,这可能表明还存在调制也可以治疗机制,“马说。
展望未来,马和Jaenisch计划探讨自身免疫免疫机制在人类利用诱导多能干细胞的1型糖尿病患者。“这些细胞可以分化成免疫细胞如T、B、巨噬细胞和树突细胞,我们可以调查他们如何相互作用β细胞,”妈妈说。
他们还计划不断改善他们的新实验系统。“这个系统提供了一个非常健壮且易处理的合成免疫反应,我们可以使用它来研究1型糖尿病,”Jaenisch说。“在未来它可以用来研究自身免疫性疾病。"
更多信息:海特马等。人类T细胞表达CD19 CAR-T受体提供洞察人类机制CD19-Positiveβ细胞破坏,细胞医学报告(2020)。DOI: 10.1016 / j.xcrm.2020.100097